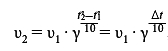Как решать термохимические уравнения
химэко
Меню сайта
Категории каталога
Форма входа
Приветствую Вас Гость!
Поиск
Друзья сайта
Наш опрос
Статистика
Термохимические уравнения включают в себя кроме химических формул тепловой эффект реакции. Числовое значение в уравнении реакции строго соответствует количествам веществ, участников реакции, т.е. коэффициентам. Благодаря этому соответствию, можно установить пропорциональные отношения между количеством вещества или массой и количеством теплоты в этой реакции.
Например: Термохимическое уравнение разложения малахита
Мы видим, что на разложение 1 моля малахита необходимо израсходовать 47 кДж, при этом образуется 2 моля оксида меди, 1 моль воды и 1 моль углекислого газа. Если мы затратим энергии в 2 раза больше, мы сумеем разложить 2 моля малахита, при этом получим 4 моля оксида меди, 2 моля воды и 2 моля углекислого газа.
Аналогично можно установить пропорциональные отношения, используя коэффициенты и молярные массы участников реакции. 47 кДж энергии затратится на разложение 94 г малахита, при этом выделится 160 г оксида меди, 18 г воды и 44 г углекислого газа. Пропорция несложная, но, используя массовые числа, учащиеся часто допускают расчетные ошибки, поэтому я рекомендую решать задачи с пропорциями через количество вещества.
Задача 1. Определите количество теплоты, которое выделится при образовании 120 г MgO в результате реакции горения магния, с помощью термохимического уравнения.
2 Mq + O 2 = 2 MqO + 1204 кДж
1) Определяем количества оксида магния, используя формулу для нахождения количества вещества через массу.
n ( MqO ) = 120г/ 40 г/моль = 3 моль
2) Составляем пропорцию с учетом коэффициентов в уравнении реакции
Как решать термохимические уравнения
Чтобы вскипятить чайник, требуется 315,2 кДж теплоты. Сколько граммов угля надо сжечь, чтобы получить такое количество теплоты? Примите, что уголь — это чистый углерод. Термохимическое уравнение сгорания углерода имеет вид
Ответ дайте в граммах и округлите до десятых.
Из пропорции получаем:
Чтобы нагреть воздух в двухкомнатной квартире на один градус, требуется 250 кДж теплоты. Сколько литров метана (н. у.) надо сжечь, чтобы получить такое количество теплоты? Термохимическое уравнение сгорания метана имеет вид
Ответ округлите до целых.
Из пропорции получаем:
Синтез аммиака протекает в соответствии с термохимическим уравнением реакции
Определите количество теплоты (кДж), которое выделится в результате образования 560 мл (н. у.) газообразного аммиака. (Запишите число с точностью до сотых.)
Из пропорции получаем:
Из предложенного перечня выберите все экзотермические реакции.
1) гашение оксида кальция водой
2) термическое разложение нитрата серебра
3) нейтрализация соляной кислоты гидроксидом калия
4) синтез аммиака из простых веществ
5) синтез глюкозы из углекислого газа и воды
Запишите номера выбранных ответов в порядке возрастания.
Реакции 1 и 3 являются кислотно-основными, а значит экзотермическими. Экзотермической также является реакция синтеза аммиака.
В соответствии с термохимическим уравнением
для получения 10,8 г серебра необходимо затратить теплоту в количестве
Тепловой эффект реакции в термохимическом уравнении связан с количествами вещества в соответствии с уравнением реакции. На примере этой реакции: 317 кДж затрачивается на разложение 2 моль AgNO3, образование 2 моль Ag, 2 моль NO2 и 1 моль О2.
Находим молярную массу серебра (по периодической системе). M(Ag)=108 г/моль. Из уравнения реакции видно, что образуется 2 моль серебра. Находим массу m=nM, где n-количество вещества:
m=108 г/моль*2 моль=216 г. Значит, для образования 216 г серебра потребовалась теплота 317 кДж.
Расчёты по термохимическим уравнениям
Теоретический материал представлен на страницах:
Любая химическая реакция сопровождается поглощением или выделением энергии. Термохимические уравнения показывают соотношение между кол-вом веществ, вступающих в реакцию, и кол-вом энергии, которую выделяют, либо поглощают эти вещества в процессе химической реакции.
Главное отличие термохимического уравнения от молекулярного заключается в том, что кроме формул и коэффициентов, в нем указывается еще и кол-во энергии (теплоты реакции), относящееся к числу молей реагирующих веществ, соответствующему коэффициентам в уравнении реакции.
Если известна масса одного из двух реагирующих веществ, на основе термохимического уравнения можно определить кол-во теплоты реакции.
Если известно кол-во выделенной (поглощенной) теплоты в ходе реакции, можно определить массы прореагировавших веществ.
Это очень простая задача, решение которой указано в условии.
Второй вариант записи термохимического уравнения.
Первая часть задания не вызывает трудностей:
В этом термохимическом уравнении 2 моля оксида азота образуется при взаимодействии 1 моля азота и 1 моля кислорода. Для того, чтобы переписать данное уравнение для 1 моля оксида азота, необходимо все коэффициенты и кол-во теплоты разделить на 2:
Для решения задачи воспользуемся правилом Вант-Гоффа, которое выражается следующей математической формулой:
При повышении температуры с 10 до 30 градусов Цельсия скорость реакции увеличится в 16 раз.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Тепловой эффект химической реакции. Термохимические уравнения. Расчеты теплового эффекта реакции.
Любая химическая реакция сопровождается выделением или поглощением энергии в виде теплоты.
По признаку выделения или поглощения теплоты различают экзотермические и эндотермические реакции.
Экзотермические реакции – такие реакции, в ходе которых тепло выделяется (+Q).
Эндотермические реакции – реакции, при протекании которых тепло поглощается (-Q).
Тепловым эффектом реакции (Q) называют количество теплоты, которое выделяется или поглощается при взаимодействии определенного количества исходных реагентов.
Термохимическим уравнением называют уравнение, в котором указан тепловой эффект химической реакции. Так, например, термохимическими являются уравнения:
Также следует отметить, что термохимические уравнения в обязательном порядке должны включать информацию об агрегатных состояниях реагентов и продуктов, поскольку от этого зависит значение теплового эффекта.
Расчеты теплового эффекта реакции
Пример типовой задачи на нахождение теплового эффекта реакции:
При взаимодействии 45 г глюкозы с избытком кислорода в соответствии с уравнением
выделилось 700 кДж теплоты. Определите тепловой эффект реакции. (Запишите число с точностью до целых.)
Решение:
Рассчитаем количество вещества глюкозы:
Т.е. при взаимодействии 0,25 моль глюкозы с кислородом выделяется 700 кДж теплоты. Из представленного в условии термохимического уравнения следует, что при взаимодействии 1 моль глюкозы с кислородом образуется количество теплоты, равное Q (тепловой эффект реакции). Тогда верна следующая пропорция:
0,25 моль глюкозы — 700 кДж
Из этой пропорции следует соответствующее ей уравнение:
Решая которое, находим, что:
Таким образом, тепловой эффект реакции составляет 2800 кДж.
Расчёты по термохимическим уравнениям
Намного чаще в заданиях ЕГЭ по термохимии значение теплового эффекта уже известно, т.к. в условии дается полное термохимическое уравнение.
Рассчитать в таком случае требуется либо количество теплоты, выделяющееся/поглощающееся при известном количестве реагента или продукта, либо же, наоборот, по известному значению теплоты требуется определить массу, объем или количество вещества какого-либо фигуранта реакции.
Пример 1
В соответствии с термохимическим уравнением реакции
образовалось 68 г оксида алюминия. Какое количество теплоты при этом выделилось? (Запишите число с точностью до целых.)
Решение
Рассчитаем количество вещества оксида алюминия:
В соответствии с термохимическим уравнением реакции при образовании 4 моль оксида алюминия выделяется 3330 кДж. В нашем же случае образуется 0,6667 моль оксида алюминия. Обозначив количество теплоты, выделившейся при этом, через x кДж составим пропорцию:
Данной пропорции соответствует уравнение:
Решая которое, находим, что x = 555 кДж
Т.е. при образовании 68 г оксида алюминия в соответствии с термохимическим уравнением в условии выделяется 555 кДж теплоты.
Пример 2
В результате реакции, термохимическое уравнение которой
выделилось 1655 кДж теплоты. Определите объем (л) выделившегося диоксида серы (н.у.). (Запишите число с точностью до целых.)
Решение
В соответствии с термохимическим уравнением реакции при образовании 8 моль SO2 выделяется 3310 кДж теплоты. В нашем же случае выделилось 1655 кДж теплоты. Пусть количество вещества SO2, образовавшегося при этом, равняется x моль. Тогда справедливой является следующая пропорция:
8 моль SO2 — 3310 кДж
x моль SO2 — 1655 кДж
Из которой следует уравнение:
Решая которое, находим, что:
Таким образом, количество вещества SO2, образовавшееся при этом, составляет 4 моль. Следовательно, его объем равен:
V(SO2) = Vm ∙ n(SO2) = 22,4 л/моль ∙ 4 моль = 89,6 л ≈ 90 л (округляем до целых, т.к. это требуется в условии.)
Больше разобранных задач на тепловой эффект химической реакции можно найти здесь.
Тепловой эффект химической реакции. Термохимические уравнения
Разделы: Химия
Тип урока: комбинированный урок.
Тема урока: « Тепловой эффект химической реакции. Термохимические уравнения».
Цель урока: дать понятие учащимся о термохимических уравнениях, познакомить с решением задач на нахождение теплового эффекта химической реакции.
Задачи урока:
Образовательные: сформировать знания учащихся о термохимических уравнениях, тепловом эффекте химической реакции, экзотермической реакции, эндотермической реакции; научить решать задачи по термохимическим уравнениям; повторить химические свойства кислорода, закрепить навыки составления уравнений химических реакций; закрепить понятия: оксид, бинарное соединение, реакция горения, совершенствовать умения решать задачи по химической формуле ( нахождение массовой доли элемента в веществе ); работать с таблицей Д.И. Менделеева;
Развивающие: развивать внимание, память, логическое мышление, наблюдательность; продолжать формирование умения делать выводы из проведённых наблюдений, сравнивать, совершенствовать умение высказывать и обосновывать суждение.
Воспитательные: воспитывать интерес к предмету химии, коллективизм, чувство здорового соперничества.
Методы ведения урока:
словесные (беседа, объяснение, рассказ)
наглядные (таблица химических элементов Д.И. Менделеева, ТСО, раздаточный материал, шаблоны, плакаты по технике безопасности, кроссворд
практические (демонстрация опытов)
Оборудование урока: таблица Д.И.Менделеева, плакаты по технике безопасности, ТСО, видеофильм «Химия 8» Суровцева Р.П., Гузей Л.С., раздаточный материал, шаблоны, кроссворд, доска.
Реактивы: 2 лаб. стакана, термометр, соль ( нитрат аммония ), концентрированная серная кислота, вода,
Оформление доски:
Ход урока
1) Организационный момент: сообщение темы урока, целей и задач урока
2) Проверка домашней работы:
А. Фронтальный опрос
— Какую тему мы начали изучать на предыдущих уроках? (Кислород)
— Назовите химическую формулу кислорода. (О2)
— С какими веществами взаимодействует кислород? (С простыми и сложными)
— Какие продукты получаются в результате реакций с кислородом? (Оксиды)
— Что такое оксиды? Это сложные вещества, состоящие из двух элементов, один из которых кислород)
— Что такое бинарное соединение? (Соединение, состоящее из двух элементов)
Б. Индивидуальная работа
3 ученика выполняют домашнее задание на доске
Задача № 1. ( ученик со слабой мотивацией )
Вычислите содержание элементов в оксиде серы (VI).
Задача № 2. ( ученик со средней мотивацией )
Задача № 3. ( ученик с сильной мотивацией )
Известно, что в организме человека содержится по массе 65% кислорода. Вычислите, сколько кислорода содержится в вашем организме?
Каждому из трёх учащихся задаются дополнительные теоретические вопросы по определениям, изучаемым ранее.
В. Проверка задания на доске, выставление оценок
Итог домашней работы
— Дайте названия веществам, которые встретились вам в домашней работе ( Оксид серы (VI), оксид железа ( II ), оксид железа ( III ).
— Что общего у этих веществ? ( Это сложные вещества, оксиды ).
— Как можно получить оксиды? ( Устно ).
3) Повторение темы « Кислород. Оксиды. Горение »
Письменное задание на доске ( ученик со средней мотивацией )
Итог повторения, выставление оценки
— Как называются реакции взаимодействия веществ с кислородом? ( Горение, окисление ).
— Какую химическую реакцию человек начал использовать с давних времён7 ( Горение ).
Просмотр отрывка видеофильма ( исторический факт добывания огня ).
— Для чего человеку нужен был огонь? ( Греться, готовить пищу ).
А сейчас мы узнаем, что теплота есть в любой химической реакции.
Запись в тетради новой темы урока.
4) А. Объяснение нового материала ( запись в тетради )
Демонстрационный опыт: вода + концентрированная серная кислота
Повышение температуры воды измеряем до и после реакции.
Техника безопасности при работе с серной кислотой, растворами, со стеклянной посудой, термометром.
Демонстрационный опыт: вода + соль ( нитрат аммония )
Понижение температуры воды измеряем термометром до и после добавления соли.
Техника безопасности при работе с сыпучими веществами.
Б. Решение задачи на нахождение теплового эффекта реакции (объяснение учителя )
Количество теплоты, выделившееся или поглотившееся в результате реакции можно измерить калориметром или рассчитать при помощи задачи. Например:
Задача. Какое количество теплоты выделится при сгорании 500 г угля, если тепловой эффект реакции 394 кДж?
В. Закрепление. Самостоятельная работа. ( Учащихся по вариантам выполняют решение задач по карточкам )
Вариант № 1 Вычислите количество теплоты, которое выделится при горении серы массой 32 г, если тепловой эффект реакции 310 кДж.
Вариант № 2 Вычислите количество теплоты, которое выделится при горении водорода массой 100 г, если тепловой эффект реакции 484 кДж.
При выполнении работы осуществляется индивидуальная помощь учителя.
Первые 3 работы оцениваются.
Устная проверка ( 2 ученика комментируют решение )
4) Итог урока, выставление оценок
Что нового вы узнали сегодня на уроке?
5) Закрепление
Учащимся раздаются шаблоны, где вместо пропущенных слов они должны вписать нужные слова.
7) Домашнее задание ( по учебнику ).
8) Игровой материал ( в оставшееся время учащиеся разгадывают кроссворд по теме: «Кислород».
Кроссворд ( работа с классом )
1. Сложное вещество, состоящее из двух элементов, один из которых кислород
2. Вещество, при разложении которого в лаборатории получают кислород ( бытовое название )
3. Реакция кислорода с другими веществами
4. Химический элемент, образующий газообразный оксид
5. Вещество жёлтого цвета, горящее в кислороде синим пламенем
6. Самый распространённый на Земле элемент
7. Вещество, увеличивающее скорость химической реакции
8. Вещество, применяющееся с кислородом для сварки и резки металлов
9. Свойство атомов химических элементов присоединять определённое число атомов других химических элементов
10. Оксид водорода