Как рассчитывается степень окисления
Как расставлять и как определить степень окисления элементов
В химических процессах главную роль играют атомы и молекулы, свойства которых определяют исход химических реакций. Одной из важных характеристик атома является окислительное число, которое упрощает метод учета переноса электронов в частице. Как определить степень окисления или формальный заряд частицы и какие правила необходимо знать для этого?
Определение

Термин окисление (оксидация) в химии означает реакцию, в ходе которой группа атомов или один из них теряют электроны или приобретают, в случае приобретения реакцию называют «восстановлением».
Степень окисления – это величина, которая измеряется количественно и характеризует перераспределяемые электроны в ходе реакции. Т.е. в процессе оксидации электроны в атоме уменьшаются или увеличиваются, перераспределяясь между другими взаимодействующими частицами, и уровень оксидации показывает, как именно они реорганизуются. Данное понятие тесно связано с электроотрицательностью частиц – их умением притягивать и отталкивать от себя свободные ионы.
Это интересно! Что такое алканы: строение и химические свойства
Определение уровня оксидации зависит от характеристик и свойств конкретного вещества, поэтому нельзя однозначно назвать процедуру вычисления легкой или сложной, но ее результаты помогают условно записать процессы окислительно-восстановительных реакций. Следует понимать, что полученный результат вычислений является результатом учета переноса электронов и не имеет физического смысла, а также не является истинным зарядом ядра.
Важно знать! Неорганическая химия часто использует термин валентности вместо степени окисления элементов, это не является ошибкой, но следует учитывать, что второе понятие более универсальное.
Понятия и правила вычислений движения электронов являются основой для классификации химических веществ (номенклатура), описания их свойств и составления формул связи. Но наиболее часто данное понятие используется для описания и работы с окислительно-восстановительными реакциями.
Правила определения степени окисления
Как узнать степень окисления? При работе с окислительно-восстановительными реакциями важно знать, что формальный заряд частицы всегда будет равен величине электрона, выраженного в числовом значении. Эта особенность связана с тем предположением, что электронные пары, образующие связь, всегда полностью смещаются в сторону более отрицательных частиц. Следует понимать, что речь идет об ионных связях, а в случае реакции при ковалентной связи электроны будут делиться поровну между одинаковыми частицами.
Окислительное число может иметь как положительные, так и отрицательные значения. Все дело в том, что в процессе реакции атом должен стать нейтральным, а для этого нужно либо присоединить к иону некое количество электронов, если он положительный, либо отнять их, если он отрицательный. Для обозначения данного понятия при записи формулы обычно прописывают над обозначением элемента арабскую цифру с соответствующим знаком. Например, 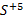
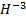
Следует знать, что формальный заряд металлов всегда будет положительным, а в большинстве 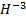
Запомнив эти особенности, достаточно просто будет определять окислительное число у элементов, независимо от сложности и количества уровней атомов.
Полезное видео: определение степени окисления
Как определить степень окисления
Периодическая таблица Менделеева содержит почти всю необходимую информацию для работы с химическими элементами. Например, школьники используют только ее для описания химических реакций. Так, чтобы определить максимальные положительные и отрицательные значения окислительного числа необходимо свериться с обозначением химического элемента в таблице:
Таким образом, достаточно просто узнать крайние границы формального заряда того или иного элемента. Такое действие можно совершить с помощью вычислений на основе таблицы Менделеева.
Важно знать! У одного элемента могут быть одновременно несколько различных показателей оксидации.
Различают два основных способа определения уровня оксидации, примеры которых представлены ниже. Первый из них – это способ, который требует знаний и умений применять законы химии. Как расставлять степени окисления с помощью этого способа?

Для этого необходимо:
Это интересно! Уроки химии: что это такое галогены
Этот способ весьма хорош, поскольку правильность решения всегда можно проверить, если сложить все уровни оксидации вместе.
Второй метод можно применять без знания химических законов:
Рассмотрим второй метод на примере вещества Na2SO4, в котором не определен атом серы S, известно лишь, что он отличен от нуля.
Это интересно! Уроки химии: катионы и анионы – что это такое
Чтобы найти, чему равны все степени окисления необходимо:
Таким образом, чтобы использовать второй метод, достаточно знать простые законы арифметики.
Таблица оксидации
Для простоты работы и вычисления показателей оксидации для каждого химического вещества используют специальные таблицы, где прописаны все данные.
Она выглядит следующим образом:
Полезное видео: учимся определять степень окисления по формулам
Вывод
Нахождение степени окисления для химического вещества – это простое действие, которое требует лишь внимательности и знания основных правил и исключений. Зная исключения и пользуясь специальными таблицами, это действие не будет занимать много времени.
Что это такое
В химии описание различных окислительно-восстановительных процессов не обходится без степеней окисления – специальных условных величин, при помощи которых можно определить заряд атома какого-либо химического элемента.
Если представить степень окисления (не путайте с валентностью, так как во многих случаях они не совпадают) как запись в тетради, то мы увидим просто цифры со знаками ноль (0 – в простом веществе), плюс (+) или минус (-) над интересующим нас веществом. Как бы то ни было, они играют огромную роль в химии, а умение определять СО(степень окисления) – это необходимая база в изучении данного предмета, без которой дальнейшие действия смысла не имеют.
Мы используем СО, чтобы описать химические свойства вещества (или отдельного элемента), верного написания его международного названия (понятного для любой страны и нации вне зависимости от используемого языка) и формулы, а также для классификации по признакам.
Степень может быть трёх видов: высшая (для её определения требуется знать, в какой группе находится элемент), промежуточная и низшая (необходимо из числа 8 вычесть номер группы, в которой располагается элемент; естественно, цифра 8 берётся потому, что всего в периодической системе Д.Менделеева 8 групп). Подробно об определении степени окисления и правильном её расставлении будет сказано ниже.
Как определяется степень окисления: постоянная СО
Во-первых, СО может быть переменной или постоянной
Определение постоянной степени окисления не составляет большого труда, поэтому урок лучше начинать именно с неё: для этого необходимо только умение пользоваться ПС (периодической системой). Итак, существует ряд определённых правил:
На основе данных сведений расставляются степени окисления во множестве сложных веществ, описываются окислительно-восстановительные реакции и прочее, однако об этом позже.
Переменная СО
Некоторые химические элементы отличаются тем, что имеют не одну степень окисления и меняют её в зависимости от того, в какой формуле стоят. Согласно правилам сумма всех степеней также должна равняться нулю, но для её нахождения необходимо проделать некоторые вычисления. В письменном варианте это выглядит как просто алгебраическое уравнение, но со временем мы «набиваем руку», и не составляет труда составить и быстро выполнить весь алгоритм действий мысленно.
Разобраться на словах будет не так легко, и лучше сразу перейти к практике:
Дополнительные упражнения можно будет найти в конце, но прежде всего нам требуется определить, какие элементы имеют переменную степень окисления. В принципе, все элементы, не считая первых трёх групп, меняют свои степени. Наиболее ярким примером служат галогены (элементы VII группы, не считая фтора F), IV группа и благородные газы. Ниже вы увидите перечень некоторых металлов и неметаллов с переменной степенью:
Это лишь небольшое количество элементов. Чтобы научиться определять СО, требуется изучение и практика, однако это не значит, что нужно заучивать все постоянные и переменные СО наизусть: просто запомните, что последние встречаются значительно чаще. Зачастую немалую роль играет коэффициент и то, какое вещество представлено – к примеру, в сульфидах отрицательную степень принимает сера (S), в оксидах – кислород (O), в хлоридах – хлор (Cl). Следовательно, в этих солях положительную степень принимает другой элемент (и называется в данной ситуации восстановителем).
Решение задач на определение степени окисления
Теперь мы подошли к самому главному – практике. Попробуйте выполнить следующие задания сами, а затем посмотрите разборку решения и сверьте ответы:
Краткое заключение
Чтобы научиться определять степень окисления самостоятельно, вам нужно не только уметь составлять уравнения, но и основательно взяться за изучение свойств элементов различных групп, вспомнить уроки алгебры, составляя и решая уравнения с неизвестной переменной.
Не забывайте, что в правилах есть свои исключения и о них нельзя забывать: речь идёт об элементах с переменной СО. Также для решения многих задач и уравнений необходимо умение расставлять коэффициенты (и знать, с какой целью это делается).
Как ⭐️ определить степень окисления
Классификация
Видео
Как расставлять степени окисления в органических соединениях
Пример 6. Укажите степени окисления всех элементов в CH3CH2OH.
Степень окисления
Степень окисления – условный заряд атома химического элемента в соединении, рассчитанный исходя из предположения, что все связи в его молекуле ионные, т.е. все связывающие электронные пары смещены к атомам с большей электроотрицательностью.
Как рассчитать степень окисления элемента в соединении?
1) Степень окисления химических элементов в простых веществах всегда равна нулю.
2) Существуют элементы, проявляющие в сложных веществах постоянную степень окисления:
| Щелочные металлы, т.е. все металлы IA группы — Li, Na, K, Rb, Cs, Fr | +1 |
| Все элементы II группы, кроме ртути: Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd | +2 |
| Алюминий Al | +3 |
| Фтор F | -1 |
3) Существуют химические элементы, которые проявляют в подавляющем большинстве соединений постоянную степень окисления. К таким элементам относятся:
| водород H | +1 | Гидриды щелочных и щелочно-земельных металлов, например:  |
| кислород O | -2 | Пероксиды водорода и металлов:  Фторид кислорода — Фторид кислорода —  |
4) Алгебраическая сумма степеней окисления всех атомов в молекуле всегда равна нулю. Алгебраическая сумма степеней окисления всех атомов в ионе равна заряду иона.
5) Высшая (максимальная) степень окисления равна номеру группы. Исключения, которые не попадают под это правило, — элементы побочной подгруппы I группы, элементы побочной подгруппы VIII группы, а также кислород и фтор.
Химические элементы, номер группы которых не совпадает с их высшей степенью окисления (обязательные к запоминанию)
| Кислород | VI | +2 (в OF2) |
| Фтор | VII | |
| Медь | I | +2 |
| Железо | VIII | +6 (например K2FeO4) |
6) Низшая степень окисления металлов всегда равна нулю, а низшая степень окисления неметаллов рассчитывается по формуле:
низшая степень окисления неметалла = №группы − 8
Отталкиваясь от представленных выше правил, можно установить степень окисления химического элемента в любом веществе.
Решение:
Запишем формулу серной кислоты:
Степень окисления водорода во всех сложных веществах +1 (кроме гидридов металлов).
Обозначим степень окисления серы как x:
Молекула серной кислоты, как и молекула любого вещества, в целом электронейтральна, т.к. сумма степеней окисления всех атомов в молекуле равна нулю. Схематически это можно изобразить следующим образом:
Т.е. мы получили следующее уравнение:
Таким образом, степень окисления серы в серной кислоте равна +6.
Пример 2
Определите степень окисления всех элементов в дихромате аммония.
Решение:
Запишем формулу дихромата аммония:
Как и в предыдущем случае, мы можем расставить степени окисления водорода и кислорода:
Однако мы видим, что неизвестны степени окисления сразу у двух химических элементов — азота и хрома. Поэтому найти степени окисления аналогично предыдущему примеру мы не можем (одно уравнение с двумя переменными не имеет единственного решения).
Мы знаем степени окисления водорода и кислорода. Зная, что сумма степеней окисления атомов всех элементов в ионе равна заряду, и обозначив степени окисления азота и хрома как x и y соответственно, мы можем записать:
Т.е. мы получаем два независимых уравнения:
Решая которые, находим x и y:
Как определять степени окисления элементов в органических веществах можно почитать здесь.
Как определить степень окисления в органических соединениях
Несколько простых примеров на определение степеней окисления
Пример 1. Необходимо найти степени окисления элементов в аммиаке (NH3).
Видео
Как расставлять степени окисления в органических соединениях
Пример 6. Укажите степени окисления всех элементов в CH3CH2OH.
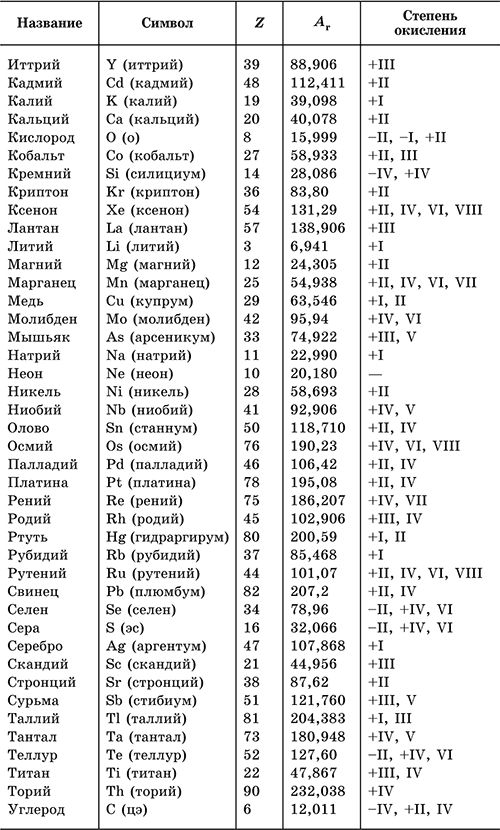
Таблица степени окисления химических элементов
Максимальную положительную и минимальную отрицательную степень окисления можно определить с помощью Периодической таблицы Д.И. Менделеева. Они равны номеру группы, в которой расположен элемент, и разнице между значением «высшей» степени окисления и числом 8, соответственно.
Если рассматривать химические соединения более конкретно, то в веществах с неполярными связями степень окисления элементов равна нулю (N2, H2, Cl2).
Степень окисления металлов в элементарном состоянии равна нулю, так как распределение электронной плотности в них равномерно.
При определении степени окисления элементов в соединениях с полярными ковалентными связями сравнивают значениях их электроотрицательностей. Поскольку при образовании химической связи электроны смещаются к атомам более электроотрицательных элементов, то последние имеют в соединениях отрицательную степень окисления.
Существуют элементы, для которых характерно только одно значение степени окисления (фтор, металлы IA и IIA групп и т.д.). Фтор, характеризующийся наибольшим значением электроотрицательности, в соединениях всегда имеет постоянную отрицательную степень окисления (-1).
Щелочные и щелочноземельные элементы, для которых свойственно относительно невысокое значение электроотрицательности, всегда имеют положительную степень окисления, равную соответственно (+1) и (+2).
Однако, имеются и такие химические элементы, для которых характерны несколько значений степени окисления (сера – (-2), 0, (+2), (+4), (+6) и др.).
Для того, чтобы легче было запомнить сколько и какие степени окисления характерны для конкретного химического элемента используют таблицы степеней окисления химических элементов, которые выглядят следующим образом:
Русское / англ. название
(+2), редко (+1), (+3) и (+4)
+1, +2, редко (+3)
(+3), редко (+2)
(-4), (+2), (+4)
(-3), (+3), (+5), редко (+2)
(-2), (+4), (+6), редко (+2)
(-1), (+1), (+5), редко (+3), (+4)
(+4), редко (+2) и (+3)
(+3), (+5), редко (+2) и (+4)
(+3), (+6), редко (+2), (+3) и (+5)
(+3), (+4), (+8), редко (+2), (+6) и (+7)
(+4), редко (+2), (+3) и (+6)
(+2), (+4), редко (+6)
(+1), редко (+2) и (+3)
(+2), редко (+1)
(+3), редко (+1) и (+2)
(-3), (+3), (+5), редко (+4)
(-2), (+4), (+6), редко (+2)
(-1), (+1), (+5), (+7), редко (+3), (+4)
(+3), редко (+2)
(+3), редко (+2)
(+3), редко (+2)
(+3), редко (+2)
(+5), редко (+3), (+4)
(+6), редко (+2), (+3), (+4) и (+5)
(+2), (+4), (+6), (+7), редко (-1), (+1), (+3), (+5)
(+3), (+4), (+6), (+8), редко (+2)
(+3), (+4), (+6), редко (+1) и (+2)
(+2), (+4), (+6), редко (+1) и (+3)
(+1), (+3), редко (+2)
(+1), (+3), редко (+2)
(+3), редко (+3), (+2), (+4) и (+5)
(+2), (+4), редко (-2) и (+6)
(+3), (+4), (+6), редко (+2) и (+5)
Как расставить коэффициенты в окислительно-восстановительных реакциях с органическими веществами
Итак, начнем с самых простых окислительно-восстановительных реакций, в которых реагентами выступают органические соединения. Для определения степени окисления углерода будем использовать выше описанный метод. В каждом конкретном примере на этом останавливаться уже не будем.
Пример 1. СН4 + О2 → СО2 + Н2О
При расстановке коэффициентов в данном случае лучше воспользоваться методом электронного баланса:
1) определим с.о. элементов;
2) составим схемы полуреакций с элементами, изменяющими свою с.о.;
3) используя данные по числу отданных и принятых электронов в полуреакциях, найдем наименьшее общее кратное и определим множители для каждой из полуреакций;
4) просуммируем полуреакции с учетом найденных множителей (коэффициентов);
5) перенесем коэффициенты в схему реакции, поставив их перед соответствующими веществами;
6) подберем коэффициенты для всех остальных химических элементов;
7) помним, что баланс количества атомов кислорода проверяем в последнюю очередь. Обычно, если число атомов кислорода слева (до стрелки) и справа (после стрелки) сходится, то это означает, что реакция составлена правильно и все остальные коэффициенты верны.
Пример 2. С3Н8 + О2 → СО2 + Н2О
В данном случае также удобнее использовать метод электронного баланса.
Пример 3. Н2C2O4 + KMnO4 → СО2 + K2CO3 + MnO2 + Н2О
Для расстановки коэффициентов вновь воспользуемся методом электронного баланса.
Пример 4. CH3OH + K2Cr2O7 + H2SO4 → HCOOH + Cr2(SO4)3 + K2SO4 + Н2О
В данном случае метанол и дихромат калия реагируют в кислой среде. Для расстановки коэффициентов можно воспользоваться любым из методов. Еще раз применим метод электронного баланса.
Пример 5. C6H12O6 + KMnO4 + H2SO4 → CO2 + MnSO4 + K2SO4 + Н2О
Расставим коэффициенты тремя разными способами.
Способ 2. Расставим коэффициенты методом электронного баланса, используя все три с.о. углерода.
Способ 3. Поскольку реакция между глюкозой и перманганатом калия проходит в кислой среде (в H2SO4), расставим коэффициенты ионно-электронным методом (полуреакций):
1) молекулярные вещества (а к ним относится и глюкоза) на ионы не диссоциируют, поэтому в схемах полуреакций записываются в исходном виде;
2) количество недостающих кислорода и водорода в полуреакциях компенсируем, дописывая по необходимости молекулы воды H2O или ионы водорода Н + ;
3) считаем слева и справа в каждой полуреакции суммарный заряд (он создается ионами, образовавшимися при диссоциации реагирующих веществ, и ионами водорода Н + );
4) разницу зарядов компенсируем отдаваемыми или принимаемыми электронами;
5) так же, как и в методе электронного баланса, находим наименьшее общее кратное, определяем множители для каждой из полуреакций;
6) просуммируем полуреакции с учетом найденных множителей (коэффициентов);
7) перенесем коэффициенты в схему реакции, поставив их перед соответствующими веществами;
8) подберем коэффициенты для всех остальных химических элементов;
9) помним, что баланс количества атомов кислорода проверяем в последнюю очередь.
Пример 6. C3H4 + KMnO4 + H2SO4 → CH3COOH + CO2 + MnSO4 + K2SO4 + Н2О
Такое разнообразие степеней окисления одного элемента затрудняет применение метода электронного баланса. Поэтому лучше воспользоваться методом полуреакций.
Действие окислителей на органические вещества
В зависимости от строения и состава органических веществ (разветвленность углеродного скелета, наличие функциональных групп и их количество), а также от условий процесса (избыток или недостаток окислителя, его концентрация, рН раствора, нагревание или охлаждение) окисление происходит по-разному.
Так, например, при окислении алкена раствором KMnO4 в мягких условиях (без нагревания и в нейтральной или слабощелочной среде) образуется двухатомный спирт. А при окислении алкена раствором KMnO4 в жестких условиях (с нагреванием и в кислой или сильнощелочной среде) молекула по двойной связи разрушается, и образуются совершенно иные продукты. Это могут быть и карбоновая кислота, и ее соль и СО2.
Знание действия окислителей на органические вещества тех или иных классов поможет верно определить продукты окислительно-восстановительной реакции и правильно расставить в них коэффициенты.
Итак, ответ на вопрос: «Как определить степень окисления в органических веществах», – позволяет правильно составить схему реакции с участием органических веществ и подобрать наиболее оптимальный метод расстановки коэффициентов.