Как рассчитать протоны нейтроны электроны
Химические элементы
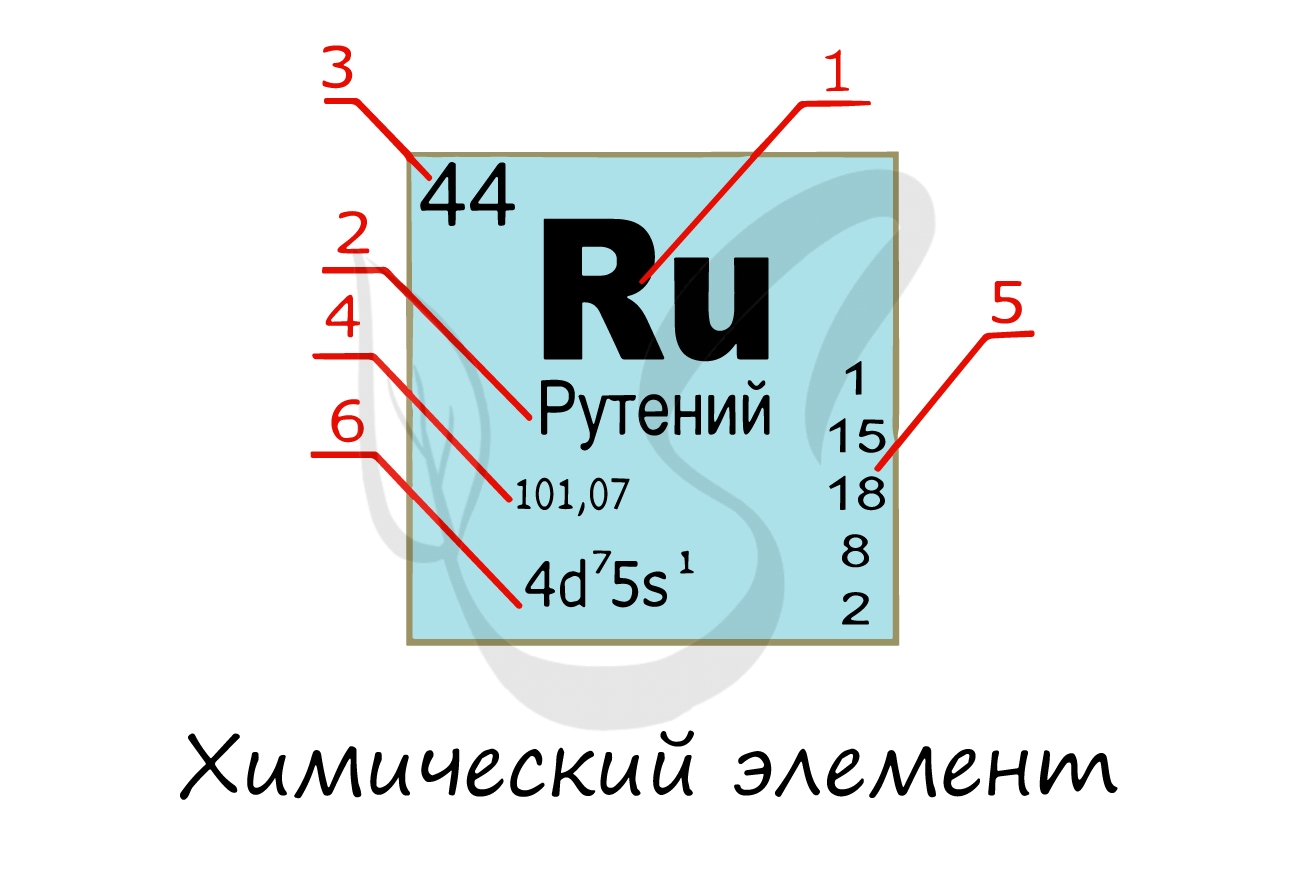
Химический элемент
Надо заметить, что на экзамене часто из карточки элемента скрывают распределение электронов и конфигурацию внешнего уровня. Тем не менее, если вы успешно освоили предыдущую тему, то для вас не составит труда написать электронную конфигурацию атома зная его порядковый номер в таблице Д.И. Менделеева (номер уж точно не тронут!))
Протоны, нейтроны и электроны
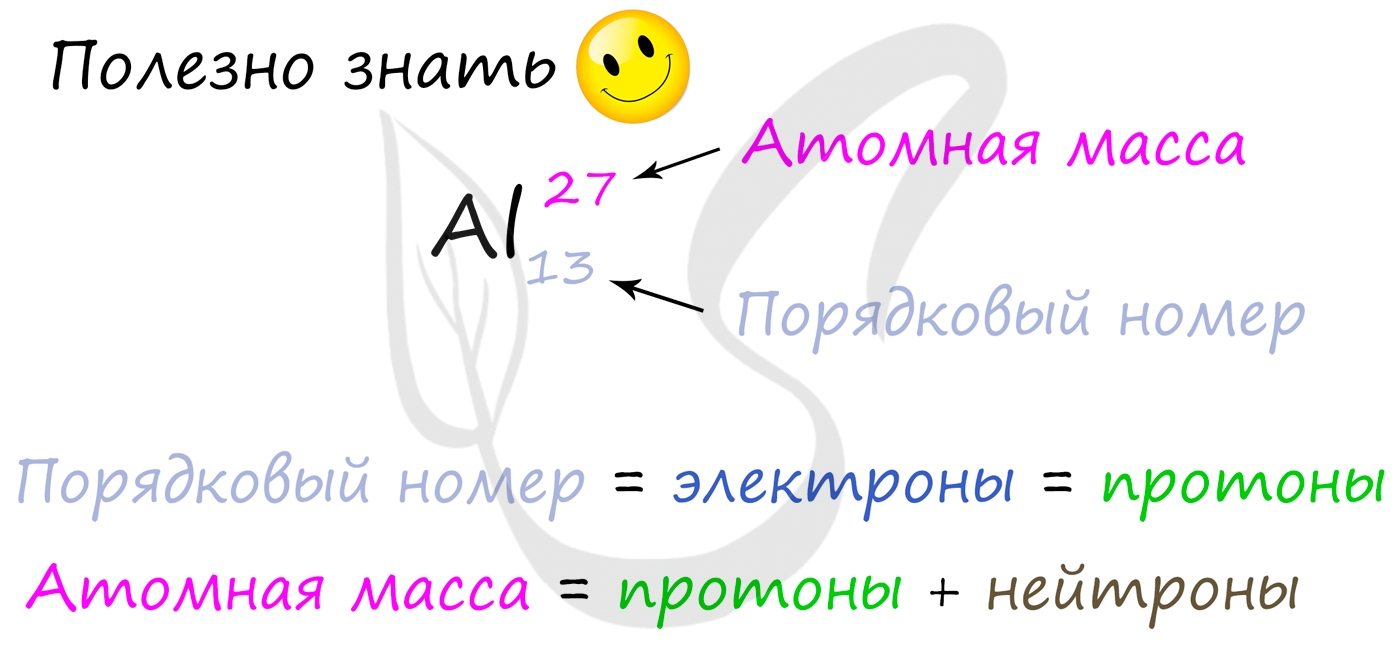
Вы уже знаете, что порядковый номер элемента в периодической таблице Д.И. Менделеева равен числу протонов, а число протонов равно числу электронов.
Для того чтобы найти число нейтронов в атоме алюминия, необходимо вычесть из атомной массы число протонов:
Получается, что в атоме алюминия 14 нейтронов. Посчитайте число нейтронов, электронов и протонов самостоятельно для атомов бериллия, кислорода, меди. Решение вы найдете ниже.
Если вы поняли суть и научились считать протоны, нейтроны и электроны, самое время приступать к следующей теме.
Изотопы
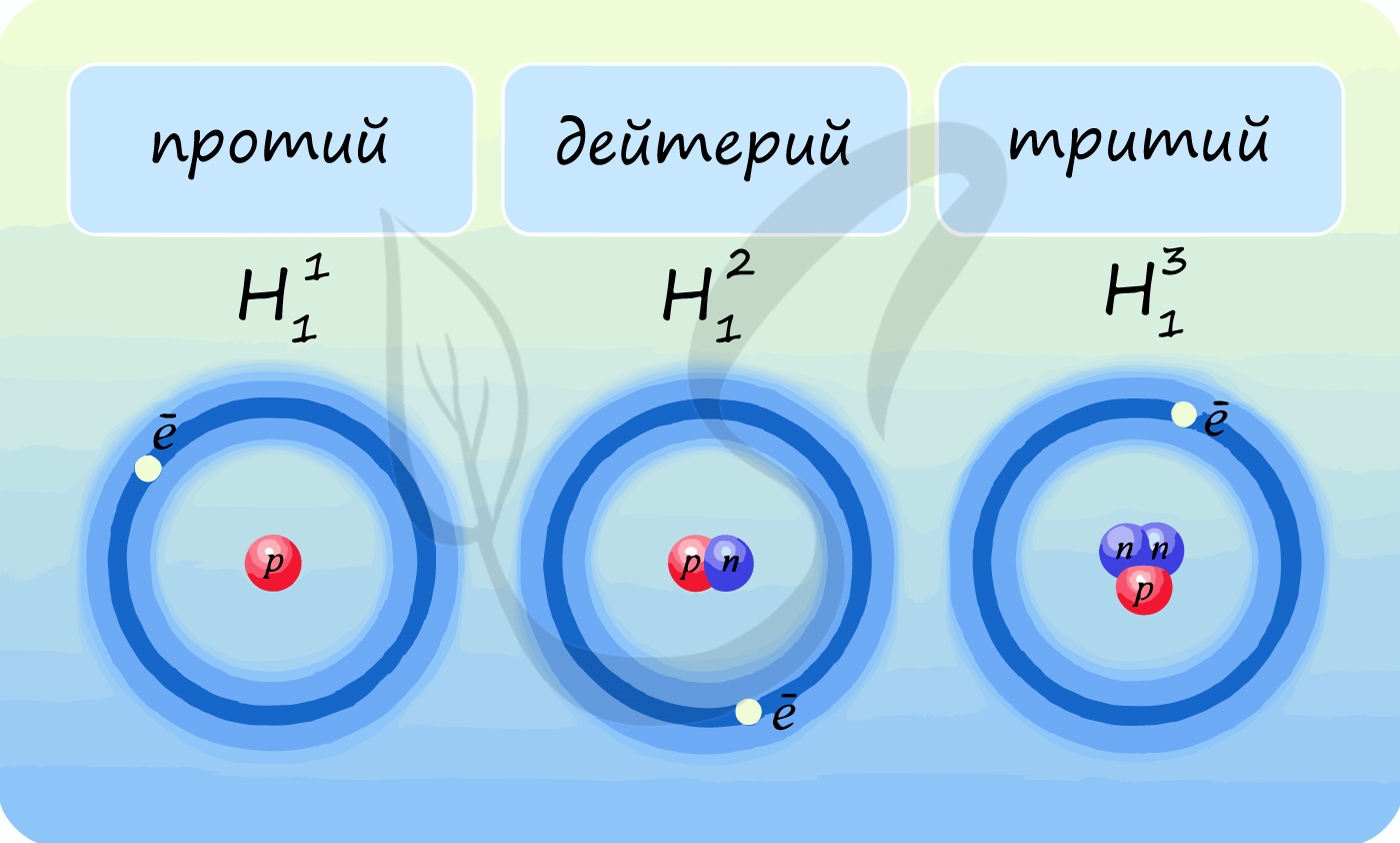
Лучше всего объяснить, что такое изотопы наглядным примером. Широко известны три изотопа водорода: протий, дейтерий и тритий.
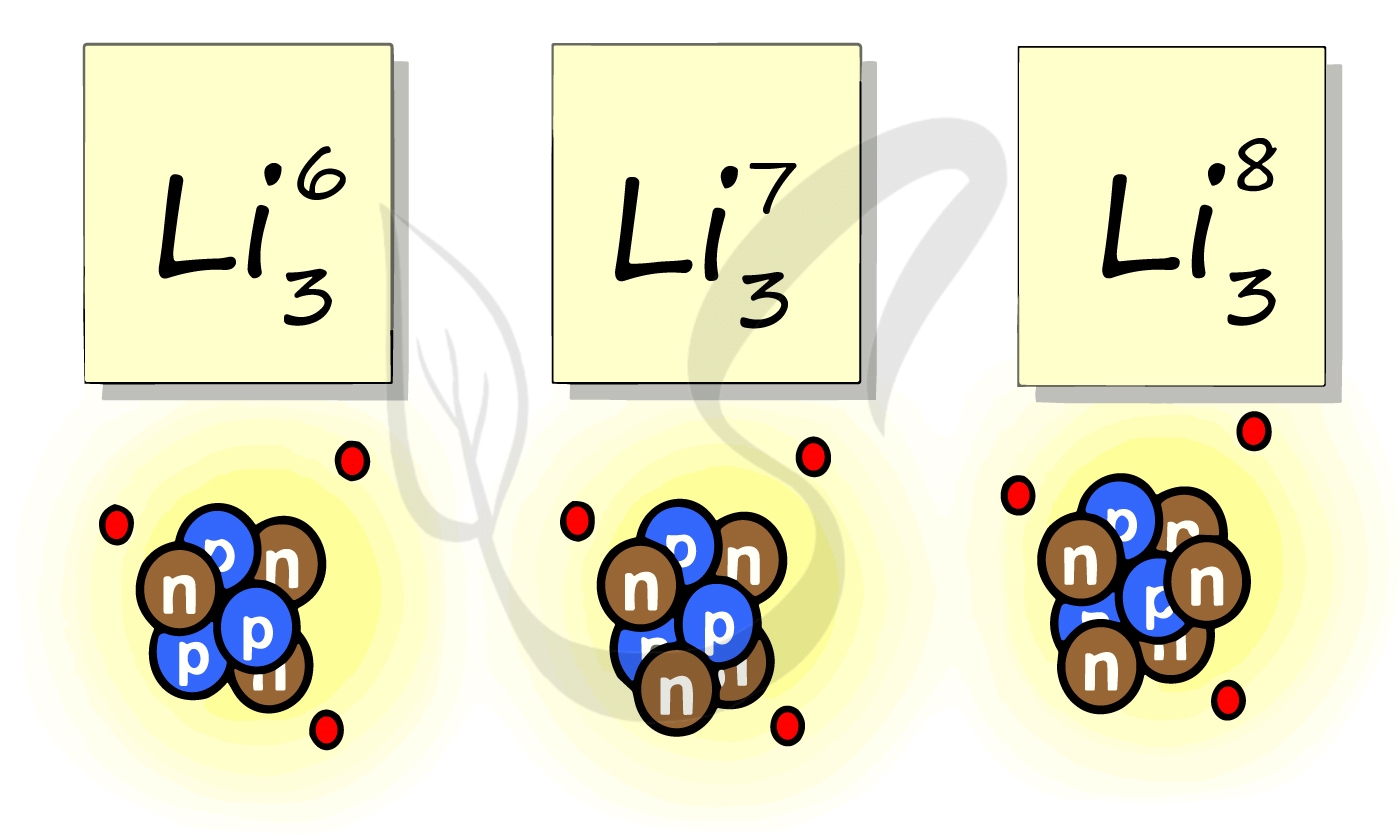
Рассмотрим пример с изотопами лития. Самостоятельно посчитайте количество нейтронов у каждого изотопа. Найдите тот, который включен в таблицу Д.И. Менделеева.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Число протонов, нейтронов и определение заряда ядра: список примеров
Содержание:
Атом – частица, которая включает протоны, нейтроны и электроны. Совокупность протонов и нейтронов атома формирует ядро, вокруг которого движутся электроны. Все элементы, содержащиеся в атоме, имеют свои особенности.
Строение атомного ядра
У протонов и нейтронов масса примерно одинакова и равна 1. Они схожи по строению, но различны по заряду. Протоны обладают положительным зарядом, а нейтроны – нулевым. Сумма протонов и нейтронов в одном атоме называется массовым числом.
Порядковый номер атома кремния равен 14. Таким образом, заряд ядра атома кремния равен 14. Ядро составляют 14 протонов и 14 нейтронов. Массовое число кремния равно 28.
Электроны
Электроны, главное число которых равно одному (n=1), размещаются на первом энергетическом уровне. Изменение главного квантового числа связано со скачкообразным изменением энергии. При этом электроны могут переходить на следующий уровень. Максимальное число электронов на энергетическом уровне определяется по формуле:
Например, на первом энергетическом уровне согласно формуле может располагаться только два электрона, а на втором – восемь электронов.
Электроны, находящиеся на внешнем уровне, слабо связаны с атомным ядром, поэтому при химических взаимодействиях эти электроны легко отсоединяются. В электронейтральных атомах число электронов соответствует его порядковому номеру.
Сколько электронов в электронейтральном атоме кремния, можно узнать по порядковому номеру элемента. Таким образом, у кремния 14 электронов.
Как рассчитать протоны нейтроны электроны
Атом состоит из ядра и вращающихся вокруг ядра электронов.
Ядро состоит из протонов и нейтронов
Протон- положительно заряженная частица
масса протона равна единице, заряд протона равен единице
Нейтрон-нейтральная частица
масса нейтрона равна единице, заряд нейтрона равен нулю
Масса атома складывается из числа протонов и числа нейтронов, масса электрона не учитывается
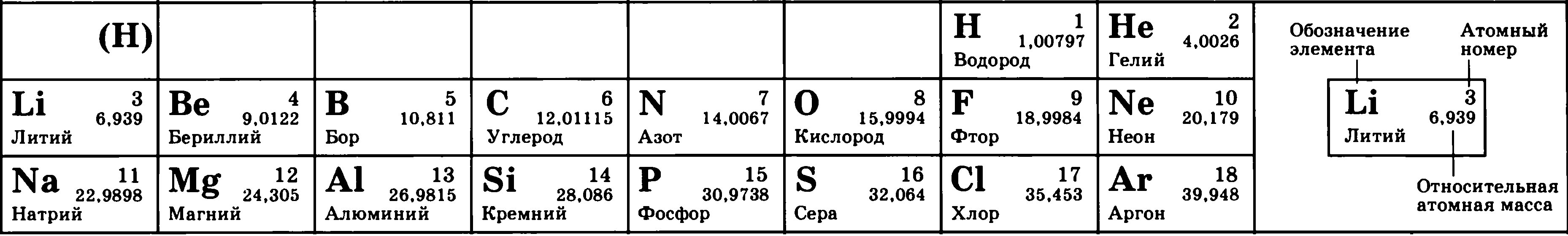
Рассмотрим фрагмент таблицы Менделеева и найдем количество протонов, нейтронов и электронов в атоме водорода
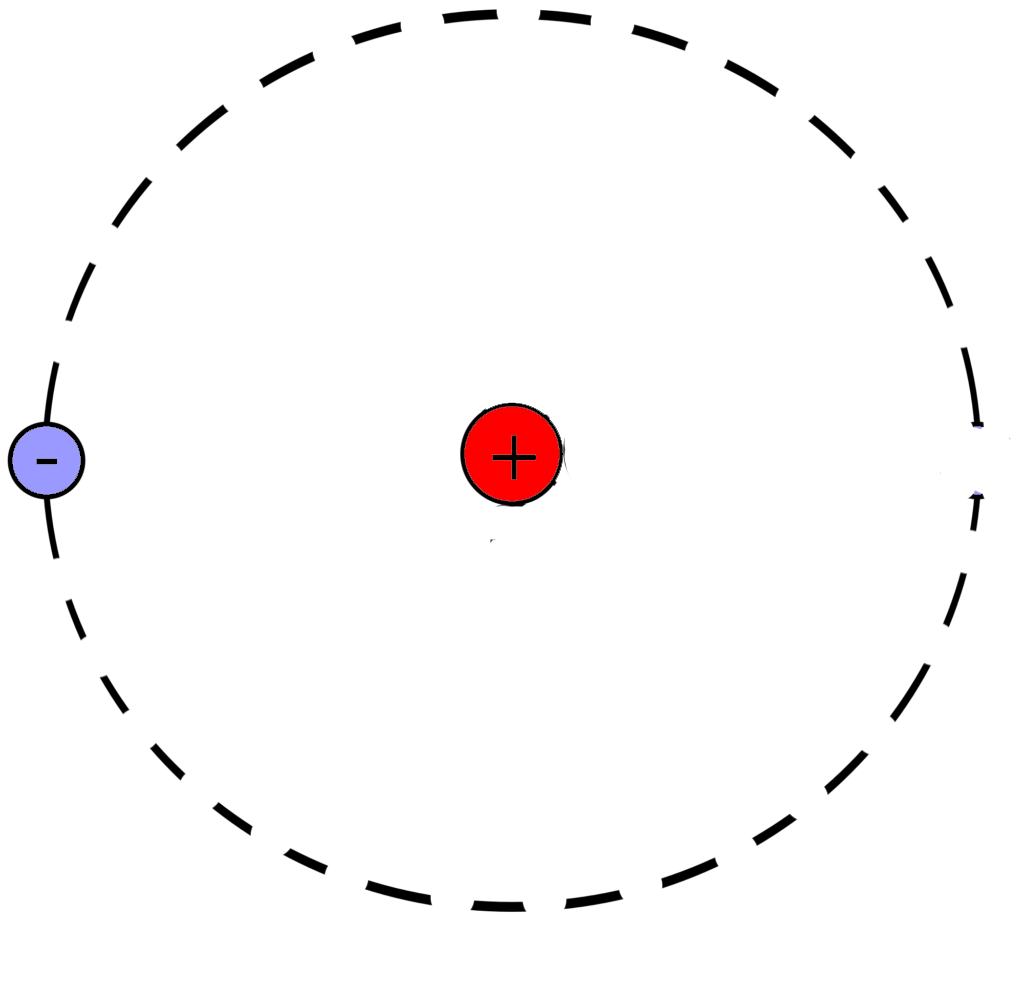
После чего начертим модель атома водорода
Порядковый номер атома водорода равен единице, значит атом имеет:
1 электрон
1 протон
Для нахождения количества нейтронов нужно из массы вычесть число протонов
Масса атома водорода равна единице
В атоме водорода нет нейтронов
Модель атома водорода:
Рассмотрим фрагмент таблицы Менделеева и найдем количество протонов, нейтронов и электронов в атоме гелия
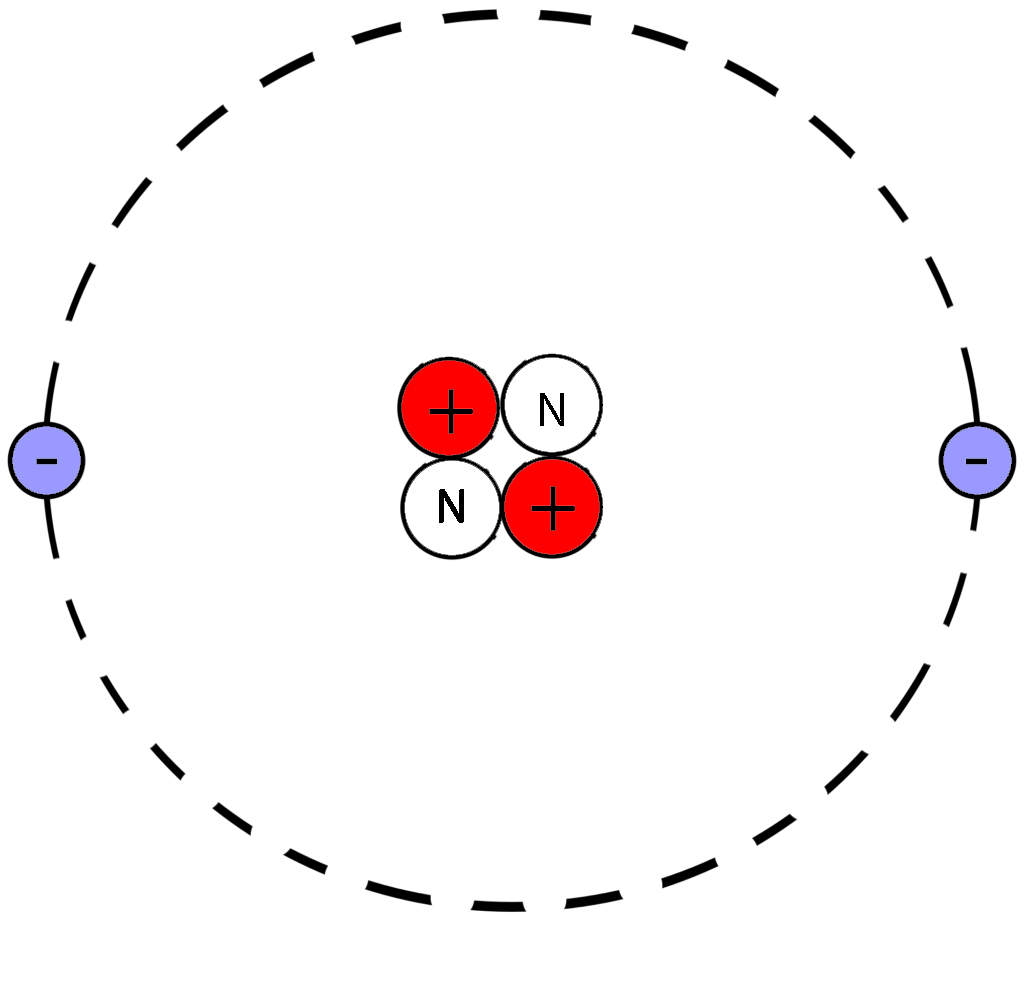
После чего начертим модель атома гелия
Порядковый номер атома гелия равен 2, значит атом имеет:
2 электрона
2 протона
Для нахождения количества нейтронов нужно из массы вычесть число протонов
Масса атома гелия равна 4
В атоме гелия 2 нейтрона
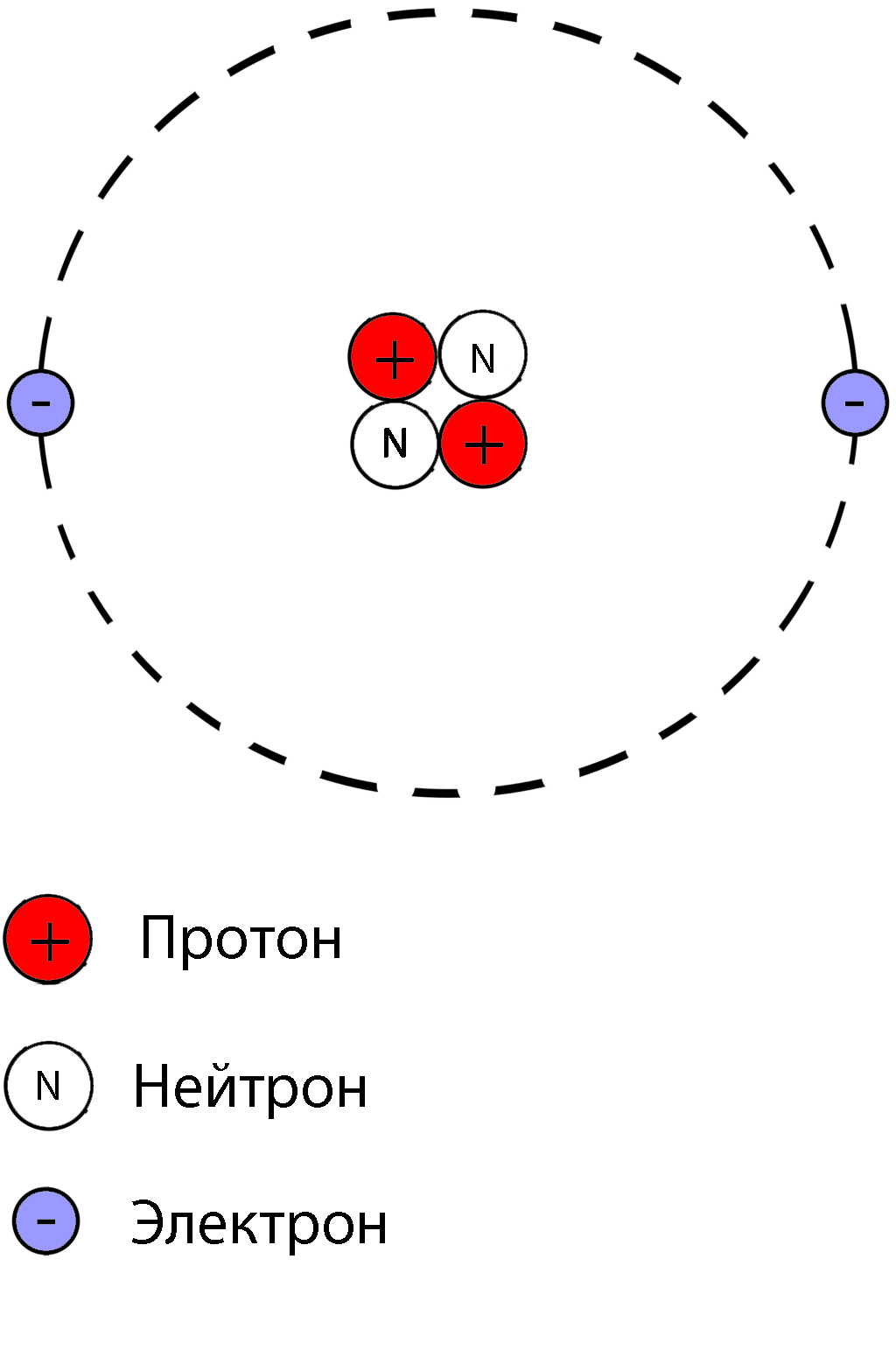
Модель атома гелия:
С помощью фрагмента таблицы Менделеева найти количество протонов, нейтронов и электронов в атоме лития
Массу атома округлить до 7.
Число протонов нейтронов электронов в атоме элемента (Таблица)
Число протонов нейтронов и электронов в атоме химического элемента (изотопа) можно определить, зная порядковый номер элемента в периодической таблице Менделеева и его атомную массу:
— Число протонов = число электронов = порядковый номер элемента
— Число нейтронов = атомная масса – число протонов
Вычислим число нейтронов в атоме на примере кислорода 16 O:
Таблица число протонов нейтронов электронов в атоме химического элемента
Справочная таблица содержит список элементов (изотопов) и их число протонов, нейтронов и электронов, а также атомную массу изотопа.
| Элемент, изотоп | Число протонов (= электронов) | Число нейтронов | Атомная масса изотопа |
| 1 H | 1 | 0 | 1,0078 |
| 2 H | 1 | 1 | 2,0141 |
| 3 He | 2 | 1 | 3,0160 |
| 4 He | 2 | 2 | 4,0026 |
| 6 Li | 3 | 3 | 6,0151 |
| 7 Li | 3 | 4 | 7,0160 |
| 9 Be | 4 | 5 | 9,0122 |
| 10 B | 5 | 5 | 10,0129 |
| 11 B | 5 | 6 | 11,0093 |
| 12 C | 6 | 6 | 12,0000 |
| 13 C | 6 | 7 | 13,0034 |
| 14 N | 7 | 7 | 14,0031 |
| 15 N | 7 | 8 | 15,0001 |
| 16 O | 8 | 8 | 15,9949 |
| 17 O | 8 | 9 | 16,9991 |
| 18 O | 8 | 10 | 17,9992 |
| 19 F | 9 | 10 | 18,9984 |
| 20 Ne | 10 | 10 | 19,9924 |
| 21 Ne | 10 | 11 | 20,9938 |
| 22 Ne | 10 | 12 | 21,9914 |
| 23 Na | 11 | 12 | 22,9898 |
| 24 Mg | 12 | 12 | 23,9850 |
| 25 Mg | 12 | 13 | 24,9858 |
| 26 Mg | 12 | 14 | 25,9826 |
| 27 Al | 13 | 14 | 26,9815 |
| 28 Si | 14 | 14 | 27,9769 |
| 29 Si | 14 | 15 | 28,9765 |
| 30 Si | 14 | 16 | 29,9738 |
| 31 P | 15 | 16 | 30,9738 |
| 32 S | 16 | 16 | 31,9721 |
| 33 S | 16 | 17 | 32,9715 |
| 34 S | 16 | 18 | 33,9679 |
| 36 S | 16 | 20 | 35,9671 |
| 35 Cl | 17 | 18 | 34,9689 |
| 37 Cl | 17 | 20 | 36,9659 |
| 36 Ar | 18 | 18 | 35,9675 |
| 38 Ar | 18 | 20 | 37,9627 |
| 40 Ar | 18 | 22 | 39,9624 |
| 39 K | 19 | 20 | 38,9637 |
| 40 K* | 19 | 21 | 39,9640 |
| 41 K | 19 | 22 | 40,9618 |
| 40 Ca | 20 | 20 | 39,9626 |
| 42 Ca | 20 | 22 | 41,9586 |
| 43 Ca | 20 | 23 | 42,9588 |
| 44 Ca | 20 | 24 | 43,9555 |
| 46 Ca | 20 | 26 | 45,9537 |
| 48 Ca* | 20 | 28 | 47,9525 |
| 45 Sc | 21 | 24 | 44,9559 |
| 46 Ti | 22 | 24 | 45,9526 |
| 47 Ti | 22 | 25 | 46,9518 |
| 48 Ti | 22 | 26 | 47,9479 |
| 49 Ti | 22 | 27 | 48,9479 |
| 50 Ti | 22 | 28 | 49,9448 |
| 50 V* | 23 | 27 | 49,9472 |
| 51 V | 23 | 28 | 50,9440 |
| 50 Cr | 24 | 26 | 49,9460 |
| 52 Cr | 24 | 28 | 51,9405 |
| 53 Cr | 24 | 29 | 52,9406 |
| 54 Cr | 24 | 30 | 53,9389 |
| 55 Mn | 25 | 30 | 54,9380 |
| 54 Fe | 26 | 28 | 53,9396 |
| 56 Fe | 26 | 30 | 55,9349 |
| 57 Fe | 26 | 31 | 56,9354 |
| 58 Fe | 26 | 32 | 57,9333 |
| 59 Co | 27 | 32 | 58,9332 |
| 58 Ni | 28 | 30 | 57,9353 |
| 60 Ni | 28 | 32 | 59,9308 |
| 61 Ni | 28 | 33 | 60,9311 |
| 62 Ni | 28 | 34 | 61,9283 |
| 64 Ni | 28 | 36 | 63,9280 |
| 63 Cu | 29 | 34 | 62,9296 |
| 65 Cu | 29 | 36 | 64,9278 |
| 64 Zn | 30 | 34 | 63,9291 |
| 66 Zn | 30 | 36 | 65,9260 |
| 67 Zn | 30 | 37 | 66,9271 |
| 68 Zn | 30 | 38 | 67,9248 |
| 70 Zn | 30 | 40 | 69,9253 |
| 69 Ga | 31 | 38 | 68,9256 |
| 71 Ga | 31 | 40 | 70,9247 |
| 70 Ge | 32 | 38 | 69,9242 |
| 72 Ge | 32 | 40 | 71,9221 |
| 73 Ge | 32 | 41 | 72,9235 |
| 74 Ge | 32 | 42 | 73,9212 |
| 75 As | 33 | 42 | 74,9216 |
| 74 Se | 34 | 40 | 73,9225 |
| 76 Se | 34 | 42 | 75,9192 |
| 77 Se | 34 | 43 | 76,9199 |
| 78 Se | 34 | 44 | 77,9173 |
| 80 Se | 34 | 46 | 79,9165 |
| 82 Se * | 34 | 48 | 81,9167 |
| 79 Br | 35 | 44 | 78,9183 |
| 81 Br | 35 | 46 | 80,9163 |
| 78 Kr * | 36 | 42 | 77,9204 |
| 80 Kr | 36 | 44 | 79,9164 |
| 82 Kr | 36 | 46 | 81,9135 |
| 83 Kr | 36 | 47 | 82,9141 |
| 84 Kr | 36 | 48 | 83,9115 |
| 86 Kr | 36 | 50 | 85,9106 |
| 85 Rb | 37 | 48 | 84,9118 |
| 87 Rb* | 37 | 50 | 86,9092 |
| 84 Sr | 38 | 46 | 83,9134 |
| 86 Sr | 38 | 48 | 85,9093 |
| 87 Sr | 38 | 49 | 86,9089 |
| 88 Sr | 38 | 50 | 87,9056 |
| 89 Y | 39 | 50 | 88,9058 |
| 90 Zr | 40 | 50 | 89,9047 |
| 91 Zr | 40 | 51 | 90,9056 |
| 92 Zr | 40 | 52 | 91,9050 |
| 94 Zr | 40 | 54 | 93,9063 |
| 93 Nb | 41 | 52 | 92,9064 |
| 92 Mo | 42 | 50 | 91,9068 |
| 94 Mo | 42 | 52 | 93,9051 |
| 95 Mo | 42 | 53 | 94,9058 |
| 96 Mo | 42 | 54 | 95,9047 |
| 97 Mo | 42 | 55 | 96,9060 |
| 98 Mo | 42 | 56 | 97,9054 |
| 100 Mo* | 42 | 58 | 99,9075 |
| 96 Ru | 44 | 52 | 95,9076 |
| 98 Ru | 44 | 54 | 97,9053 |
| 99 Ru | 44 | 55 | 98,9059 |
| 100 Ru | 44 | 56 | 99,9042 |
| 101 Ru | 44 | 57 | 100,9056 |
| 102 Ru | 44 | 58 | 101,9043 |
| 104 Ru | 44 | 60 | 103,9054 |
| 103 Rh | 45 | 58 | 102,9055 |
| 102 Pd | 46 | 56 | 101,9056 |
| 104 Pd | 46 | 58 | 103,9040 |
| 105 Pd | 46 | 59 | 104,9051 |
| 106 Pd | 46 | 60 | 105,9035 |
| 108 Pd | 46 | 62 | 107,9039 |
| 110 Pd | 46 | 64 | 109,9052 |
| 107 Ag | 47 | 60 | 106,9051 |
| 109 Ag | 47 | 62 | 108,9048 |
| 106 Cd | 48 | 58 | 105,9065 |
| 108 Cd | 48 | 60 | 107,9042 |
| 110 Cd | 48 | 62 | 109,9030 |
| 111 Cd | 48 | 63 | 110,9042 |
| 112 Cd | 48 | 64 | 111,9028 |
| 113 Cd* | 48 | 65 | 112,9044 |
| 114 Cd | 48 | 66 | 113,9034 |
| 116 Cd* | 48 | 68 | 115,9048 |
| 113 In | 49 | 64 | 112,9041 |
| 115 In* | 49 | 66 | 114,9039 |
| 112 Sn | 50 | 62 | 111,9048 |
| 114 Sn | 50 | 64 | 113,9028 |
| 115 Sn | 50 | 65 | 114,9033 |
| 116 Sn | 50 | 66 | 115,9017 |
| 117 Sn | 50 | 67 | 116,9030 |
| 118 Sn | 50 | 68 | 117,9016 |
| 119 Sn | 50 | 69 | 118,9033 |
| 120 Sn | 50 | 70 | 119,9022 |
| 122 Sn | 50 | 72 | 121,9034 |
| 124 Sn | 50 | 74 | 123,9053 |
| 121 Sb | 51 | 70 | 120,9038 |
| 123 Sb | 51 | 72 | 122,9042 |
| 120 Te | 52 | 68 | 119,9040 |
| 122 Te | 52 | 70 | 121,9030 |
| 123 Te | 52 | 71 | 122,9043 |
| 124 Te | 52 | 72 | 123,9028 |
| 125 Te | 52 | 73 | 124,9044 |
| 126 Te | 52 | 74 | 125,9033 |
| 128 Te* | 52 | 76 | 127,9045 |
| 130 Te* | 52 | 78 | 129,9062 |
| 127 I | 53 | 74 | 126,9045 |
| 124 Xe* | 54 | 70 | 123,9059 |
| 126 Xe | 54 | 72 | 125,9043 |
| 128 Xe | 54 | 74 | 127,9035 |
| 129 Xe | 54 | 75 | 128,9048 |
| 130 Xe | 54 | 76 | 129,9035 |
| 131 Xe | 54 | 77 | 130,9051 |
| 132 Xe | 54 | 78 | 131,9042 |
| 134 Xe | 54 | 80 | 133,9054 |
| 136 Xe* | 54 | 82 | 135,9072 |
| 133 Cs | 55 | 78 | 132,9055 |
| 130 Ba* | 56 | 74 | 129,9063 |
| 132 Ba | 56 | 76 | 131,9051 |
| 134 Ba | 56 | 78 | 133,9045 |
| 135 Ba | 56 | 79 | 134,9057 |
| 136 Ba | 56 | 80 | 135,9046 |
| 137 Ba | 56 | 81 | 136,9058 |
| 138 Ba | 56 | 82 | 137,9052 |
| 138 La* | 57 | 81 | 137,9071 |
| 139 La | 57 | 82 | 138,9064 |
| 136 Ce | 58 | 78 | 135,9072 |
| 138 Ce | 58 | 80 | 137,9060 |
| 140 Ce | 58 | 82 | 139,9054 |
| 142 Ce | 58 | 84 | 141,9092 |
| 141 Pr | 59 | 82 | 140,9077 |
| 142 Nd | 60 | 82 | 141,9077 |
| 143 Nd | 60 | 83 | 142,9098 |
| 144 Nd* | 60 | 84 | 143,9101 |
| 145 Nd | 60 | 85 | 144,9126 |
| 146 Nd | 60 | 86 | 145,9131 |
| 148 Nd | 60 | 88 | 147,9169 |
| 150 Nd* | 60 | 90 | 149,9209 |
| 144 Sm | 62 | 82 | 143,9120 |
| 147 Sm* | 62 | 85 | 146,9149 |
| 148 Sm* | 62 | 86 | 147,9148 |
| 149 Sm | 62 | 87 | 148,9172 |
| 150 Sm | 62 | 88 | 149,9173 |
| 152 Sm | 62 | 90 | 151,9197 |
| 154 Sm | 62 | 92 | 153,9222 |
| 151 Eu* | 63 | 88 | 150,9199 |
| 153 Eu | 63 | 90 | 152,9212 |
| 152 Gd* | 64 | 88 | 151,9198 |
| 154 Gd | 64 | 90 | 153,9209 |
| 155 Gd | 64 | 91 | 154,9226 |
| 156 Gd | 64 | 92 | 155,9221 |
| 157 Gd | 64 | 93 | 156,9240 |
| 158 Gd | 64 | 94 | 157,9241 |
| 160 Gd | 64 | 96 | 159,9271 |
| 159 Tb | 65 | 94 | 158,9253 |
| 156 Dy | 66 | 90 | 155,9243 |
| 158 Dy | 66 | 92 | 157,9244 |
| 160 Dy | 66 | 94 | 159,9252 |
| 161 Dy | 66 | 95 | 160,9269 |
| 162 Dy | 66 | 96 | 161,9268 |
| 163 Dy | 66 | 97 | 162,9287 |
| 164 Dy | 66 | 98 | 163,9292 |
| 165 Ho | 67 | 98 | 164,9303 |
| 162 Er | 68 | 94 | 161,9288 |
| 164 Er | 68 | 96 | 163,9292 |
| 166 Er | 68 | 98 | 165,9303 |
| 167 Er | 68 | 99 | 166,9320 |
| 168 Er | 68 | 100 | 167,9324 |
| 170 Er | 68 | 102 | 169,9355 |
| 169 Tm | 69 | 100 | 168,9342 |
| 168 Yb | 70 | 98 | 167,9339 |
| 170 Yb | 70 | 100 | 169,9348 |
| 171 Yb | 70 | 101 | 170,9363 |
| 172 Yb | 70 | 102 | 171,9364 |
| 173 Yb | 70 | 103 | 172,9382 |
| 174 Yb | 70 | 104 | 173,9389 |
| 176 Yb | 70 | 106 | 175,9426 |
| 175 Lu | 71 | 104 | 174,9408 |
| 176 Lu* | 71 | 105 | 175,9427 |
| 174 Hf* | 72 | 102 | 173,9400 |
| 176 Hf | 72 | 104 | 175,9414 |
| 177 Hf | 72 | 105 | 176,9432 |
| 178 Hf | 72 | 106 | 177,9437 |
| 179 Hf | 72 | 107 | 178,9458 |
| 180 Hf | 72 | 108 | 179,9466 |
| 181 Ta | 73 | 108 | 180,9480 |
| 180 W* | 74 | 106 | 179,9467 |
| 182 W | 74 | 108 | 181,9482 |
| 183 W | 74 | 109 | 182,9502 |
| 184 W | 74 | 110 | 183,9509 |
| 186 W | 74 | 112 | 185,9544 |
| 185 Re | 75 | 110 | 184,9530 |
| 187 Re* | 75 | 112 | 186,9558 |
| 184 Os | 76 | 108 | 183,9525 |
| 186 Os* | 76 | 110 | 185,9538 |
| 187 Os | 76 | 111 | 186,9558 |
| 188 Os | 76 | 112 | 187,9558 |
| 189 Os | 76 | 113 | 188,9581 |
| 190 Os | 76 | 114 | 188,9581 |
| 192 Os | 76 | 116 | 191,9615 |
| 191 Ir | 77 | 114 | 190,9606 |
| 193 Ir | 77 | 116 | 191,9626 |
| 190 Pt* | 78 | 112 | 189,9599 |
| 192 Pt | 78 | 114 | 191,9610 |
| 194 Pt | 78 | 116 | 193,9627 |
| 195 Pt | 78 | 117 | 194,9648 |
| 196 Pt | 78 | 118 | 195,9650 |
| 198 Pt | 78 | 120 | 197,9679 |
| 197 Au | 79 | 118 | 196,9666 |
| 196 Hg | 80 | 116 | 195,9658 |
| 198 Hg | 80 | 118 | 197,9668 |
| 199 Hg | 80 | 119 | 198,9683 |
| 200 Hg | 80 | 120 | 199,9683 |
| 201 Hg | 80 | 121 | 200,9703 |
| 202 Hg | 80 | 122 | 201,9706 |
| 204 Hg | 80 | 124 | 203,9735 |
| 203 Tl | 81 | 122 | 202,9723 |
| 205 Tl | 81 | 124 | 204,9744 |
| 204 Pb | 82 | 122 | 203,9730 |
| 206 Pb | 82 | 124 | 205,9745 |
| 207 Pb | 82 | 125 | 206,9759 |
| 208 Pb | 82 | 126 | 207,9767 |
| 209 Bi* | 83 | 126 | 208,9804 |
| 232 Th* | 90 | 142 | 232,0381 |
| 235 U* | 92 | 143 | 235,0439 |
* это нестабильные изотопы и с большим периодом полураспада, который равняется возрасту Вселенной.