дюфастон или циклодинон что лучше
Менопаузальная гормонотерапия (МГТ)

Почему же процент женщин, принимающих МГТ, остается невысоким?
Крупное американское исследование WHI (Women’s Health Initiative, 2002 г.) вызвало драматический период в судьбе менопаузальной гормонзаместительной терапии, что способствовало резкому сокращению МГТ в большинстве стран мира, появлению страхов и сомнений в отношении пользы и рисков.
Преждевременное завершение части исследования по менопаузальной гормонзаместительной терапии (МГТ) привлекло к себе всеобщее внимание. Как женщины, так и врачи чувствовали себя обманутыми, так как терапия, которая до этого считалась полезной для здоровья в долгосрочной перспективе, теперь оказалась опасной. Отличающийся от фактического изложения пресс-релиз предварительной работы прогремел в СМИ за неделю до того, как сама статья стала доступна для большинства читателей. Сообщалось, что исследование было остановлено в связи с повышенным риском развития рака молочной железы, связанным с заместительной гормональной терапией. На самом деле, в скорректированном анализе связь МГТ и рака молочной железы не была статистически значима!
Последующий углубленный анализ результатов WHI показал, что МГТ характеризуется благоприятным профилем пользы/риска у более молодых женщин, которые начинают терапию в близкие к менопаузе сроки. Эти результаты характеризовались сходным защитным воздействием терапии в отношении ИБС и снижения общей смертности, которые были продемонстрированы ранее в крупномасштабных наблюдательных исследованиях с участием относительно молодых женщин. После WHI широкое распространение получила так называемая временная гипотеза или гипотеза «окна терапевтических возможностей», согласно которой существует различное влияние МГТ на атеросклероз и связанные с ним клинические события в зависимости от возраста женщины и времени начала использования МГТ по отношению к моменту наступления менопаузы.
Основными недостатки данного исследования являлись:
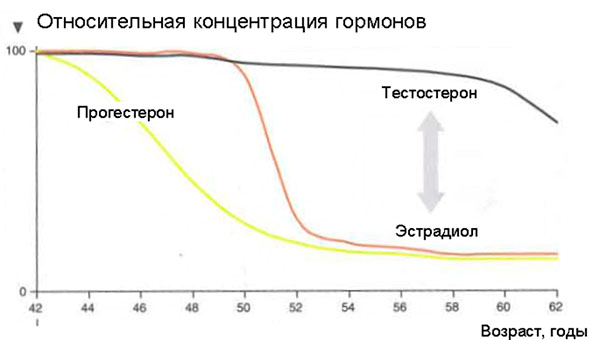
Что же происходит с женским организмом в 45-55 лет?
Что будет если МГТ не проводить?
А зачем нужно так «рисковать» и принимать «страшные» гормональные препараты при наступлении менопаузы? Ведь это естественный процесс, может, пусть все идет, как заведено природой? — Но тогда мы неизбежно столкнемся с заболеваниями, которые также предопределены природой.
Сначала появляются ранние симптомы:
Через некоторое время появятся и поздние нарушения, связанные с длительным дефицитом половых гормонов:
Какое обследование проводится перед МГТ
Перед назначением менопаузальной гормональной терапии необходимо обследование (впрочем, которое необходимо проводить хотя бы раз в год и без терапии всем сознательным женщинам старше 45 лет).
Дополнительные обследования (при соответствующих данных анамнеза):
Когда пора начинать менопаузальную гормональную терапию?
Но проблема в том, что диапазон нормы ФСГ огромен, и для каждой женщины уровень свой. В идеале нужно сдать анализы крови на гормоны в период максимального расцвета – с 19 до 23 лет. Это и будет вашей индивидуальной идеальной нормой. А начиная с 45 лет ежегодно сверять с ней результаты. Но даже если вы впервые слышите о ФСГ – лучше поздно, чем никогда: в 30, 35, 40 лет имеет смысл выяснить свой гормональный статус, чтобы ближе к критическому возрасту было, на что ориентироваться.
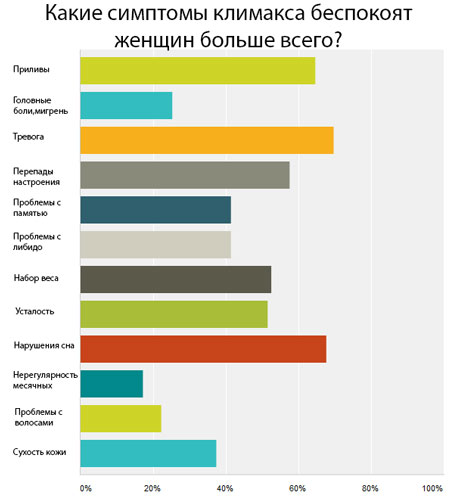
Как самостоятельно понять, что пришло время МГТ?
Уровень эстрогенов снизился, если:
Препаратов огромное количество, какие из них наиболее безопасны?
Действует принцип «минимальности» и «натуральности»!
Для менопаузальной гормональной терапии применяются различные препараты, которые могут быть разделены на несколько групп:
«Натуральные» эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному Эстрадиол–17b.
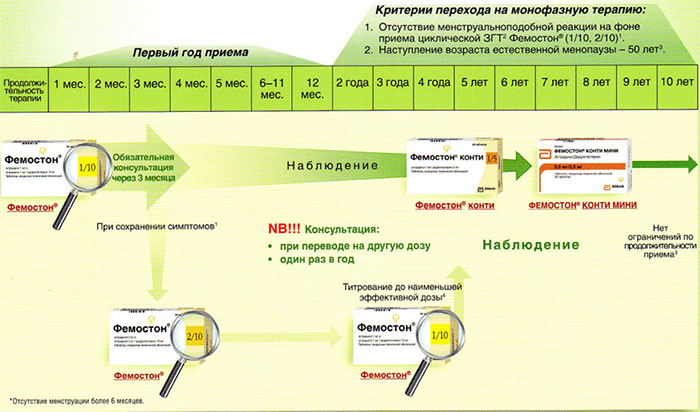
На сегодняшний день таким критериям более всего соответствует препарат Фемостон. Препараты линейки фемостона имеют различные дозировки, что укладывается в один из основных постулатов современной концепции МГТ – использование наименьшей возможной дозировки, которая сохраняет эффективность.
Препараты для двухфазной терапии – когда еще есть месячные
Фемостон 1/10 и Фемостон 2/10
В состав Фемостона 1/10 входят 28 таблеток. 14 белых, содержащих 1 мг Эстрадиола, и 14 серых, содержащих 1 мг Эстрадиола и 10 мг Дидрогестерона.
Состав Фемостона 2/10 отличается только количеством Эстрадиола
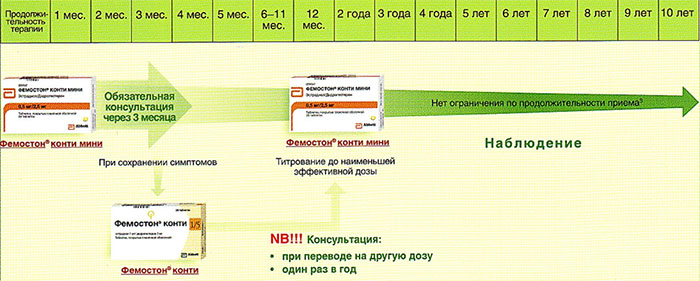
Препараты для монофазной терапии – когда месячные отсутствуют
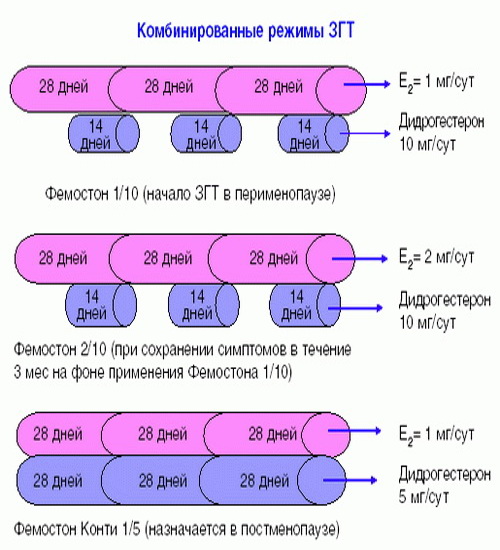
В состав Фемостона конти 1/5 входят 28 таблеток, содержащих 1 мг Эстрадиола и 5 мг Дидрогестерона.
В состав Фемостона мини 0,5/2,5 входят 28 таблеток, содержащих 0,5 мг Эстрадиола и 2,5 мг Дидрогестерона.
Ниже представлена более подробная схема первоначального назначения препаратов фемостон в пременопаузе (то есть до прекращения менструаций, но при наличии характерных климактерических симптомов). Пациенткам, у которых менструации не прекратились, рекомендуют начинать лечение в первый день менструального цикла. Пациенткам с нерегулярным менструальным циклом целесообразно начинать лечение после 10-14 дней монотерапии прогестагеном («химический кюретаж»).
Далее Вашему вниманию представлен алгоритм первоначального назначения препарата фемостон в постменопаузе (то есть когда уже прошел год и более после последней менструации).
Какой способ применения препаратов лучше?
Трансдермальное (накожное) нанесение позволяет избежать первой стадии печеночного метаболизма, благодаря чему колебания концентрации эстрадиола в плазме крови при применении накожных препаратов незначительны. Метаболизм и выведение эстрадиола при трансдермальном введении подобен метаболизму натуральных эстрогенов.
Большинству пациентов желательно использовать оптимальную и наиболее безопасную на сегодняшний день схему: Дивигель накожно + Утрожестан интравагинально.

Схема приема для женщин, у которых сохранена менструальная функция, назначается врачом. Обычно средство прописывают циклом с первого дня после окончания менструации (5 день цикла) в течение 25 дней, после овуляции (c 16 по 25 день цикла) нужно добавлять препараты гестагенов.
Утрожестан – содержит прогестерон микронизированный, существует в двух формах — 100 и 200 мг.
При МГТ в постменопаузе в непрерывном режиме препарат Утрожестан применяется в дозе 100 мг с первого дня приема эстрогенов.
При болях в молочной железе можно добавить прожестожель ежедневно по 1 дозе на каждую молочную железу 2-4 недели.
Противопоказаниями для заместительной гормонотерапии являются:
Нужен ли женщинам тестостерон?
Согласно рекомендациям Международного общества по менопаузе (International Menopause Society (IMS)) основное показание для применения тестостерона – лечение уменьшенного сексуального влечения, которое заставляет данную женщину испытывать значительные страдания. До рассмотрения вопроса о проведении терапии тестостероном необходимо решить вопросы, связанные с другими причинами нарушенного сексуального желания и/или возбуждения. К ним относятся диспареуния, депрессия, побочные эффекты лекарственных препаратов, проблемы взаимоотношений и другие проблемы со здоровьем, влияющие на женщину или ее партнера.
В настоящее время возможно применение трансдермальных препартов. На отечественном фармацевтическом рынке существует только один вариант – Андрогель, но его применение у женщин является «off-label», то есть не разрешено инструкцией. Обычно назначается 1/5 пакета в день (то есть 1 г геля/10 мг тестостерона).
Еще более перспективным может стать интравагинальная форма тестостерона, которая также может оказывать благоприятное действие при лечении вульвовагинальной атрофии.
Ключевые положения по применению препаратов тестостерона
Самые частые заблуждения:
А как же рак молочной железы, ведь это самая главная причина смерти у женщин?
В этом утверждении много заблуждений. На самом деле рак молочной железы – причина смертности в 4% случаев. Ведущая причина преждевременной смерти – сердечно-сосудистые заболевания (50%), которые запускает инсулинорезистентность. А она возникает на фоне гормональных нарушений.
Гормоны вызывают побочные эффекты и от них толстеют?
Новые низкодозированные и высокоселективные препараты направлены четко на мишень. Врачи на протяжении многих лет наблюдали за тысячами женщин, которые получали МГТ? Сегодня уже есть уникальные гестагены, метаболически нейтральные, они не приводят к ожирению и вместе с тем не понижают тестостерон, если у женщины нет его избытка. Выработаны и новые схемы лечения. Иногда при применении таблеток с эстрогенами, где-то в 10% случаев, бывают головные боли и боль в венах. В этом случае они заменяются на трансдермальные формы в виде геля.
Зачем мне принимать гормоны, если у меня нет приливов и отличное самочувствие?
Вместе с падением уровня гормонов возникает риск развития возрастных болезней: повышается артериальное давление, возникает ожирение, увеличивается риск развития сахарного диабета второго типа, подагры, остеопороза и онкологических заболеваний.
Вместо таблеток лучше принимать травы и различные фитоэстрогены?
Эффективность данных препаратов по устранению вазомоторных симптомов составляет 30%, что равно эффективности плацебо. При этом данная группа препаратов никаким образом не оказывает профилактического действия на возрастные заболевания (сердечно-сосудистые, онкологические заболевания, остеопороз, ожирение и сахарный диабет).
Циклодинон таблетки : инструкция по применению
Состав
1 таблетка, покрытая пленочной оболочкой, содержит:
прутняка обыкновенного (Agnus castus) плодов экстракт сухой 4,0 мг (7-11:1);
экстрагирующее вещество: этанол 70% об.
Вспомогательные вещества: повидон 30, кремния диоксид коллоидный безводный, картофельный крахмал, лактоза моногидрат, целлюлоза микрокристаллическая, магния стеарат, тальк, титана диоксид (Е171), железа оксид желтый (Е172), индиго кармин (Е132), макрогол 6000, эудрагит RL 30D.
Описание
Круглые, двояковыпуклые таблетки, покрытые пленочной оболочкой, зелено-голубого цвета с матовой поверхностью.
Фармакологические свойства
Компоненты лекарственного средства оказывают нормализующее действие на концентрацию половых гормонов.
Основным активным компонентом лекарственного средства является прутняк обыкновенный (Agnus castus). Дофаминергические эффекты препарата, вызывая снижение продукции пролактина, устраняют гиперпролактинемию. Повышенная концентрация пролактина нарушает секрецию гонадотропинов, в результате чего могут возникнуть нарушения созревании фолликулов, овуляции и образования желтого тела, что в дальнейшем ведет к дисбалансу между эстрадиолом и прогестероном и может вызвать нарушения менструального цикла, а также мастодинию. В отличие от эстрогенов и других гормонов, пролактин оказывает также прямое стимулирующее действие на пролиферативные процессы в молочных железах, усиливая образование соединительной ткани и вызывая расширение молочных протоков. Снижение содержания пролактина приводит к обратному развитию патологических процессов в молочных железах и купирует болевой синдром. Ритмичная выработка и нормализация соотношения гонадотропных гормонов приводит к нормализации второй фазы менструального цикла.
Показания к применению
Нарушение менструального цикла, предменструальный синдром, мастодиния.
Противопоказания
Индивидуальная повышенная чувствительность к компонентам лекарственного средства, опухоли гипофиза, карцинома молочной железы.
Применение в период беременности или кормления грудью
Лекарственное средство не следует применять женщинам во время беременности и в период кормления грудью.
Способ применения и дозировка
Принимают по 1 таблетке один раз в день, в утреннее время.
Таблетку следует проглатывать целиком, не разжёвывая, запивая достаточным количеством жидкости.
Лекарственное средство Циклодинон® следует принимать в течение нескольких месяцев без перерыва во время менструации.
После исчезновения симптомов и улучшения состояния следует продолжить лечение в течение нескольких недель.
Побочные эффекты
По данным литературных источников при приеме лекарственных средств, содержащих плоды прутняка обыкновенного, имели место такие симптомы как головная боль, зуд или нарушения со стороны желудочно-кишечного тракта (тошнота, боли в верхней или нижней части живота). Кроме того, описывались случаи повышенной чувствительности (кожная сыпь, крапивница, отек Квинке, одышка и затруднение проглатывания). Имеются данные о редких случаях преходящего психомоторного возбуждения, спутанности сознания и галлюцинаций.
При появлении первых признаков повышенной чувствительности прием лекарственного средства следует прекратить и проконсультироваться с врачом.
Опыт применения фитопрепарата «Циклодинон» («Агнукастон») у пациеток с недостаточностью функции желтого тела и гиперпролактинемией
Опубликовано в журнале:
«Проблемы репродукции», 2005, №5, с. 1-4
В.П. Сметник, Л.Б. Бутарева
Научный центр акушерства, гинекологии и перинатологии РАМН (дир. – акад. РАМН В.И. Кулаков), Москва
Представлены результаты использования фитопрепарата Циклодинон (Агнукастон), обладающего пролактинингибирующим влиянием, у пациенток репродуктивного возраста с недостаточностью функции желтого тела, обусловленной гиперпролактинемией. Терапевтическая эффективность его подтверждена нормализацией исходно повышенного уровней пролактина и пониженного прогестерона с одновременным восстановлением ритма менструаций.
Ключевые слова: пролактин, гиперпролактинемия, олигоменорея, недостаточность лютеиновой фазы, Agnus castus.
Среди многочисленных лекарственных растений, обладающих тропностью к нейроэдокринной системе человека и животных, в последнее десятилетие особое внимание уделяется Agnus Castus. Vitex agnus castus (Прутняк, «Монаший перец», Авраамово дерево), принадлежит к семейству вербеновых (Verbenaceae). Природный ареал произрастания – Средиземноморье, Крым, Африка, наиболее теплые регионы Азии и Америки.
Для лечебных целей используются плоды Agnus Castus (АК), содержащие иридоиды, флавоноиды и эфирные масла [25].
Первые упоминания об использовании вытяжек из плодов АК относят к античным временам. Подтверждения тому можно найти в работах Гиппократа (IV век до р.х.), который предписывал АК для борьбы с маточными кровотечениями и «ускорения отхождения последа».
Диоскорид Педаний, греческий военный врач и натуралист (1 в. н. э), один из основателей ботаники как науки, описал терапевтические свойства АК при воспалительных заболеваниях женских половых органов.
В народной медицине Витекс служит средством для подавления сексуального возбуждения. В своей книге о травах, изданной в 1697 г., Адам Лоницерус пишет: «Кто этими листьями устелет свое ложе, у того они отгонят все плотские соблазны». В гербариях Лоницеруса и Маттиолиса плоды и листья АК фигурируют как галактогога и аменогога [15].
В последнее время широкое применение экстрактов АК стало возможным после изучения их фармакологических свойств и открытия у пяти выделенных из липофильных фракций бициклических дитерпенов веществ, обладающих допаминергической активностью и селективным сродством к экстрогеновым рецепторам Р-подтипа. Последние, как известно, участвуют в регуляции жирового обмена, не оказывают влияния на матку и обмен в костной ткани, определяемый по уровню остеокальцина и щелочной фосфатазы [15, 18].
Многочисленные клинико-лабораторные исследования последних лет демонстрируют успешное применение АК и мастодинона, в состав которого входит АК, при лечении латентной гиперпролактинемии (ГП) и мастодинии, предменструального и климактерического синдромов [3, 17, 19].
Так, Rao G.M. et al (1997) в двойном слепом плацебо контролируемом исследовании показали, что у пациенток с циклической масталгией отмечается достоверное снижение исходно повышенного ТРГ-стимулированного уровня ПРЛ наряду с эффективностью в отношении болей в молочных железах. Кроме того, также зафиксировано параллельное со значительным повышением уровня прогестерона (Р) по сравнению с таковым при использовании плацебо увеличение вдвое продолжительности лютеиновой фазы менструального цикла [23].
Таким образом, вышеизложенные данные послужили основанием для использования фитопрепарата Циклодинон (Агнукастон) (содержащего 20 мг активного АК, фирма Бионорика АГ, Германия) у пациенток с недостаточностью функции желтого тела, обусловленной относительной гиперпролактинемией, с целью коррекции имеющихся нарушений и оценки клинической эффективности и переносимости препарата.
МАТЕРИАЛЫ И МЕТОДЫ
Комплексному клинико-лабораторному обследованию подверглись 20 пациенток в возрасте от 25 до 41 (30,0±0,9) года с относительной гиперпролактинемией и страдающих нарушениями менструального цикла различного характера.
Критериями для включения в исследование являлись:
Группу контроля составили 15 соматически здоровых женщин в возрасте от 24 до 26 лет.
У находившихся под наблюдением больных жалобы, заставившие обратиться к гинекологу, были следующими:
При выполнении работы наряду с общеклиническим обследованием, включающим подробное изучение анамнеза, особенностей менструального цикла, репродуктивной функции, общий и гинекологический осмотр, также использовали радиоиммунологические методы при исследовании сывоторочных концентраций ПРЛ, эстрадиола (Е2), Р. Учитывая наличие суточных ритмов секреции ПРЛ, забор крови осуществляли спустя 3-4 часа после пробуждения пациентки [13]. В качестве нормативных значений использовали пределы нормы, разработанные в лаборатории эндокринологии НЦ АГ и П РАМН (табл. 1).
Таблица 1. Нормативные значения концентрации гормонов в сыворотке крови
| гормон | фолликулиновая фаза (I) | лютеиновая фаза (II) |
| ПРЛ мМЕ/л | 120-500 | 120-500 |
| Е2 пмоль/л | 150-480 | 280-940 |
| Р нмоль/л | 1,8-2,2 | 9-83 |
Также как и гормональные на 4-5 и 20-21 дни спонтанной менструации всем обследованным до начала и после завершения 3-х месячной терапии Циклодиноном (Агнукастоном) производилось эхографическое исследование органов малого таза на аппарате «Aspen» (фирмы Acuson, США) с использованием мультичастотного 4,0-6,0-8,0 МГц трансвагинального датчика. Все исследования осуществлялись в первой половине суток, по методике опорожненного мочевого пузыря. С помощью этого же аппарата и линейным датчиком частотой 7-10 МГц обследовали состояние молочных желез.
Для исключения опухолевого генеза ГП магнитно-резонансно-томографическое (МРТ) обследование проводили на оборудовании «Magnetom Impact» (Siemens) c контрастным усилением «Magnevit».
При статистической обработке данных применяли прикладные программы «Статистика» пакета MATLAB 5,3. Достоверность различий в группах определена по t-критерию Стьюдента, различия считались достоверными при рОбъективизация эффективности лечения оценена путем математического расчета динамики гормональных параметров (в процентах) по формуле:
(средний начальный показатель – средний конечный показатель/средний конечный показатель) х 100% [21]
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В соответствии с поставленной целью комплексное клинико-лабораторное обследование проведено у 20 женщин (основная группа) с ГП в возрасте от 25 до 41 года (30,9±0,9 лет). По данным литературных источников, около 80% больных всех форм ГП – это молодые женщины аналогичного возрастного диапазона [5].
Средний возраст соматически здоровых женщин группы контроля составил 25,5±1,2 года. Ни одна из обследованных обеих групп не имела выраженных метаболических расстройств, о чем свидетельствует нормальный показатель индекса массы тела (18 кг/м2≤ИМТ с 25 кг/м2).
При изучении приморбидного фона у больных с ГП превышения числа перенесенных в детском возрасте инфекционных заболеваний по сравнению с таковыми у обследованных контрольной группы и данными в популяции отмечено не было (р>0,05) (табл. 2) [1].
Таблица 2. Частота перенесенных инфекционных заболеваний и сопутствующей экстрагенитальной патологии у обследованных женщин
| Нозологические формы | Основная группа (n=20) | Группа контроля (n=15) | Данные популяции (%) |
| Корь | 25% (5) | 40% (6) | 80 |
| Краснуха | 15% (3) | 13,3% (2) | 12,6% |
| Инфекционный паротит | 30% (6) | 33,3 (5) | 32,3% |
| Ветряная оспа | 30% (6) | 33,3% (5) | 41,3% |
| Скарлатина | 15% (3) | 26,6% (4) | 41,0% |
| Заболевания ЦНС (инфекционные + травмы головного мозга) | 20% (4) | 6,6% (1) | |
| Артериальная гипертензия | 15% (3) | — | |
| Заболевания органов желудочно-кишечного тракта, в том числе гепато-билиарной системы | 50% (10) | 13,3% (2) | |
| Заболевания органов мочевыделительной системы | 10% (2) | 13,3% (2) |
Вместе с тем, следует отметить, что у 20% из числа обследованных пациенток основной группы имели место заболевания ЦНС и перенесенные травмы головного мозга, после которых у трех развилась транзиторная артериальная гипертензия. Практически у каждой второй пациентки в структуре сопутствующей экстрагенитальной заболеваемости преобладала патология желудочно-кишечного тракта, в том числе гепато-билиарной системы (10 больных). В этом аспекте немаловажен тот факт, что трое из десяти пациенток в течение 2-х предшествующих настоящему обследованию лет перенесли эндоскопическую холицистэктомию по поводу желчно-каменной болезни. У трех других клинические проявления совпали с тяжелыми стрессовыми ситуациями в семье.
Наши данные, как и многочисленные указания в литературе, в том числе и эпидемиологические исследования, подтверждают значимость стрессорного фактора в развитии неопухолевой ГП [8, 16, 20, 22].
К провоцирующим моментам ГП у остальных пациенток, по-видимому, можно отнести 1,5-2-летний прием эстроген-гестагенных оральных контрацептивов. Влияние данной группы препаратов на секрецию ПРЛ общеизвестно и широко отражено в современной литературе. Как эндогенные, так и экзогенные эстрогены, входящие в состав комбинированных оральных контрацептивов и препаратов для заместительной гормонотерапии, использующихся в пери- и постменопаузальном периоде, активируют эстрогенчувствительный элемент гена ПРЛ и способствуют увеличению синтеза и секреции последнего. Оральные контрацептивы, возможно не вызывают образования пролактином, но способны стимулировать их развитие и функцию и обычно не назначаются пациенткам с такими опухолями [2, 14].
Анализ особенностей менструальной функции показал, что средняя продолжительность цикла составила 39,5±7,3 дня, длительность менструации – от 3 до 5 дней. Кроме того, 7 женщин основной группы обратились по поводу более скудных менструаций. В то время как в группе контроля межменструальный интервал не превышал 28 (26,5±1,2)дней.
Развитие вторичной олигоменореи, типичного проявления ГП, как правило, относят к дебюту заболевания и при неопухолевом генезе частота ее достигает 58,1% [10, 11, 20, 28].
Однако, в литературе имеются указания и на сохранение регулярного ритма менструаций при пятикратном превышении ПРЛ у больных с аденомой гипофиза [12, 16]. В 30-70% случаев гиперпролактинемию сопровождает бесплодие [6, 7, 8, 26].
В наших наблюдениях отсутствие беременности отмечено у 25% пациенток.
В анамнезе остальные 11 (55%) женщин имели от 2 до 6 беременностей, из которых от 1 до 3-х завершились самостоятельными своевременными родами, от 2-х до 4-х – неосложенными искусственными абортами. Остальные 4 (20%) пациентки не планировали беременность.
В процессе изучения основных гормональных параметров, характеризующих стероидную функцию яичников и пролактинсекретирующую аденогипофиза, получены данные, позволившие по степени повышения базального уровня ПРЛ всех обследованных основной группы разделить на две подгруппы (А и В). Так у 13 (65%) пациенток, отнесенных в подгруппу А, показатели среднего исходного уровня ПРЛ находились в диапазоне от 618,0 мМЕ/л до 774,0 мМЕ/л, составив в среднем 698,8 мМЕ/л. У остальных 7 (35%) – данный средний исходный параметр достигал 1066,0 мМЕ/л (1028-1098 мМЕ/л), они и составили подгруппу В. (табл. 3).
Таблица 3. Динамика содержания сывороточных уровней пролактина, эстрадиола и прогестерона до- и на фоне терапии Циклодиноном (Агукастоном)
| Гормон | Средние исходные значения | Средние конечные значения | ||
| Фазы менструального цикла | ||||
| I фаза | II фаза | I фаза | II фаза | |
| Пролактин (мМЕ/л): | ||||
| А подгруппа | 698,8 (618,0-774,0) | 713,1 (566-913) | 498,7 (531-670) | 501,6 (418-513) |
| В подгруппа | 1066,0 (1028-1098) | 1060,0 (1200-1215) | 821,6 (697-907) | 760,0 (696-810) |
| Е2 (nмоль/л): | ||||
| А подгруппа | 159,0 (95-228) | 213,9 (107-350) | ||
| В подгруппа | 163,1 (101-211) | 292,5 (157-295) | ||
| Р (нмоль/л): | ||||
| А подгруппа | 18,5 (3,1-28,1) | 28,3 (18,5-48,7) | ||
| В подгруппа | 8,7 (2,7-19,1) | 22,1 (11,4-47,1) | ||
Как видно из представленных в таблице 3 данных, достоверных различий в содержании средних исходных уровней ПРЛ в I и II фазы менструального цикла у обследованных А и В подгрупп выявлено не было (р>0,05). Однако, у 5 пациенток подгруппы А отмечалось превышение его в 1,2 раза на 20-21 день по сравнению с таковым на 4-5 дни менструального цикла. Полученные сведения согласуются с данными Ю.А. Комаровой (1986), В.П. Сметник и Л.Г. Тумилович (1995) и, по-видимому, могут свидетельствовать об определенной этиологической роли ГП в генезе наблюдаемых у данной когорты пациенток предменструальных психо-эмоциональных расстройств и выраженной циклической масталгии [12, 23].
Подтверждения данного предположения можно найти в сообщениях Nunes M. et al. (1980) также обнаруживших изменения психо-эмоциональной сферы у больных с ГП [22].
Интересен тот факт, что несмотря на объективные различия в базальных уровнях ПРЛ, средние исходные концентрации Е2 по подгруппам существенно не отличались и составили 159,0 nмоль/л для подгруппы А и 163,1 nмоль/ л для подгруппы В. Выявленные исходно пониженные по сравнению с нормативными и в группе контроля уровни Р (18,5 нмоль/л и 8,7 моль/л) – свидетельствовали о недостаточности функции желтого тела.
Вместе с тем показатели средних конечных значений уровня ПРЛ после 3-х месячой терапии Циклодиноном (Агнукастоном) заметно отличались.
Так у пациенток подгруппы А как в раннюю фолликулиновую, так и лютеиновую фазы цикла, средние конечные показатели уровня ПРЛ снизились до нормальных значений, составив 498,7 мМЕ/л и 501,6 мМЕ/л – соответственно. В то же время, как показывают результаты обследования, у 7-ми пациенток подгруппы В конечные средние показатели ПРЛ и во II и в I фазы менструального цикла не достигли нормативных отметок, а оставались повышенными от 760 мМе/л до 821,6 мМЕ/л и, соответственно.
Трем пациенткам подгруппы В с конечными показателями уровня ПРЛ от 730 до 907МЕ/л для исключения органических изменений гипофиза произведена МРТ головного мозга с контрастным усилением. Лишь в одном наблюдении картина магнитно-резонансной томографии была подозрительной в отношении микроаденомы за счет ассиметричности и неоднородности структуры гипофиза, ослабления накопления контрастного вещества. В двух других случаях – на основе проведенного исследования опухолевая природа ГП была исключена.
Объективизация эффективности лечения произведена путем математического анализа, результаты которого позволили определить степень снижения уровня ПРЛ и повышения Р для каждой из выделенных подгрупп (табл. 4).
Таблица 4. Показатели динамики сывороточных уровней пролактина и прогестерона на фоне терапии Циклодиноном (Агнукастоном)
| Подгруппы | Степень изменения (%) | |
| I фаза | II фаза | |
| Подгруппа А (n=13) | ||
| пролактин | (-) 39,9 | (-) 42,2 |
| прогестерон | (+) 34,6 | |
| Подгруппа В (n=7) | ||
| пролактин | (-) 29,7 | (-) 39,5 |
| прогестерон | (+) 60,6 | |
Анализируя приведенные выше данные можно заключить, что степени снижения средних исходных уровней ПРЛ в подгруппе А в I и II фазы менструального цикла были соизмеримы и составили 39,9% и 42,2%. В тоже время в подгруппе В отмечалось более, чем полуторократное, по сравнению с подгруппой А, повышение средних конечных показателей Р в лютеиновую фазу менструального цикла (60,6% против 34,6%; рТерапевтическая эффективность применения Циклодинона (Агнукастона) в обеих подгруппах подтверждена не только клиникой (восстановление ритма менструации) и данными эхографического мониторинга (УЗ-признаки произошедшей овуляции, наличие полноценных желтых тел), а также повышением уровней Р на 20-21 дни цикла.
Сопоставляя графики ректальной температуры с концентрацией Р нами были выявлены корреляции лишь в 35% случаев. Это еще раз подтверждает мнение о том, что базальная температура не может служить абсолютно объективным тестом, адекватно отражающим деятельность яичников.
К концу 3 месяца терапии ни в одном из наблюдений не было отмечено увеличения размеров тела матки и прогрессирования аденомиоза (3 случая I-II ст. диффузного аденомиоза), а также миоматозных узлов (2 наблюдения с межмышечным расположением последних 1-1,5 см в диаметре). Во всех случаях на момент завершения терапии состояние эндометрия соответствовало фазам менструального цикла.
Ультразвуковой мониторинг не выявил изменений в эхографической картине соотношения стромального, железистого компонентов и жировой ткани молочной железы до- и после 3-х месячного курса терапии. Вместе с тем, субъективное улучшение в отношении циклической масталгии было констатировано практически у всех 8 пациенток.
Важно отметить тот факт, что у 2 женщин (конечные показатели ПРЛ – 764,0 мМЕ/л, Р – 47 нмоль/л и 560,0 мМЕ/л, 68 нмоль/л, соответственно) страдающих вторичным бесплодием в цикле отмены спонтанно наступили беременности, завершившиеся самостоятельными своевременными родами.
В результате проводимого суточного мониторинга артериального давления резких колебаний его у пациенток как с нормо-, так и гипотонией зафиксировано не было. Всеми отмечалась хорошая переносимость препарата.
Таким образом, резюмируя предварительные данные, касающиеся использования Циклодинона (Агнукастона) у женщин репродуктивного возраста, можно сделать следующие выводы: